Auf der Suche nach dem Zwischenwirt für das SARS-CoV-2-Virus
Ob Fledermäuse das neue Coronavirus direkt auf den Menschen übertragen haben oder ob es über eine weitere Tierart, also einen Zwischenwirt, zum Menschen gelangt ist, wissen die Virologen nicht. Sie vermuten, dass ein Zwischenwirt beteiligt war oder mehrere Zwischenwirte beteiligt waren. Ein Forschungsansatz, der helfen könnte, diesen Zwischenwirt oder diese Zwischenwirte zu finden, stützt sich auf die Sequenz-und Strukturanalyse des Proteins Angiotensin-converting enzyme 2 (ACE2).
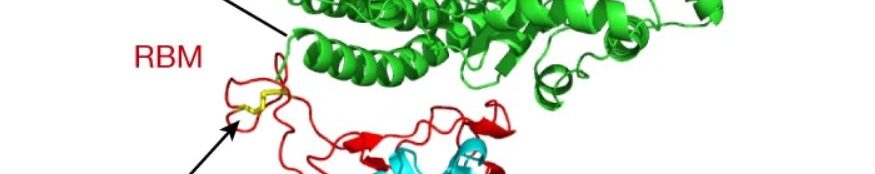
ACE2 ist der Rezeptor, den das SARS-CoV-2-Virus benutzt, um im Menschen an Zellen zu binden und in sie einzudringen. ACE21 befindet sich auf der Oberfläche verschiedener Zellen, einschließlich Epithelzellen in Nase, Mund, Lunge und Schlagadern. SARS-CoV-2 bindet mit seinem Spikeprotein (S-Protein) an ACE2. Proteinstrukturforscher haben mittels Röntgenkristallografie ein dreidimensionales Modell der Proteinstruktur von ACE2 erstellt, wenn es das Spikeprotein bindet [1] und herausgefunden, dass für die Bindung des Spikeproteins 25 Aminosäuren des ACE2s wichtig sind [2].
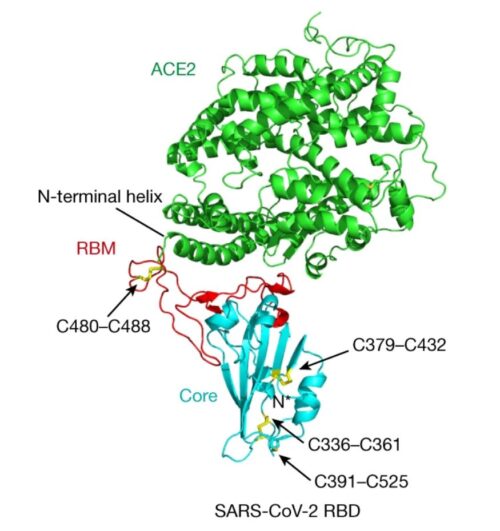
Ein internationales Team von Virologen schaute sich deshalb bei tierischen ACE2 an, ob an den 25 gleichen Stellen im Protein die gleichen 25 Aminosäuren wie beim menschlichen ACE2 zu finden sind. Die Forscher veröffentlichten die Ergebnisse ihrer Sequenzanalysen in der Fachzeitschrift PNAS [2}.
“Bei Tieren, bei denen alle 25 Aminosäuren mit denen im menschlichen Protein übereinstimmen, wird das höchste Risiko vorhergesagt, über ACE2 mit SARS-CoV-2 infiziert zu werden”, sagte Joana Damas, von der UC Davis, eine der AutorInnen des Fachartikels. “Unser Modell sagt vorher, dass das Infektionsrisiko abnimmt, je mehr sich die ACE2-Bindungs-Aminosäuren der Wirbeltierart von denen des Menschen unterscheiden.
Die Forscher verglichen die Proteinsequenz des menschlichen ACE2 mit den Proteinsequenzen von tierischen ACE2 in 410 anderen Wirbeltierarten, darunter Vögel, Fische, Amphibien, Reptilien und Säugetiere. Für Epidemiologen ist es wichtig, das Wirtsspektrum von SARS-CoV-2 zu kennen, um künftige Pandemien besser voraussagen und kontrollieren zu können. Es ist auch wichtig, um Wildtierpopulationen in einheimischen Lebensräumen und unter menschlicher Obhut zu schützen, insbesondere nicht menschliche Primaten, die für COVID-19 anfällig sein könnten.
Der Westliche Flachlandgorilla, der Sumatra-Orang-Utan und der Nördliche Weißwangen-Schopfgibbon, haben ein sehr hohes Risiko, sich über ihren ACE2-Rezeptor mit SARS-CoV-2 zu infizieren. Weitere Säugetiere, die als hochgefährdet eingestuft werden, sind Meeressäuger wie Grauwale und Tümmler sowie chinesische Hamster.
Bei Haustieren wie Katzen, Rindern und Schafen wurden ein mittleres Risiko und bei Hunden, Pferden und Schweinen ein geringes Risiko für eine Bindung des viralen Spikeproteins festgestellt. Auch Fledermäuse ein haben ein sehr geringes Risiko, sich über ihr ACE2 mit SARS-CoV-2 zu infizieren, was mit den experimentellen Daten übereinstimmt.
In dokumentierten Fällen einer SARS-CoV-2-Infektion bei Nerz, Katzen, Hunden, Hamstern, Löwen und Tigern kann das Virus ACE2-Rezeptoren verwenden oder sie können andere Rezeptoren als ACE2 verwenden, um Zugang zu den Zellen zu erhalten. Eine geringere Neigung zur Bindung könnte sich in einer geringeren Infektionsneigung oder einer geringeren Fähigkeit zur Ausbreitung der Infektion in einem Tier oder zwischen Tieren, sobald sie einmal etabliert ist, niederschlagen.
Die Autoren mahnen aber zur Vorsicht und bitten die Vorhersagen ihres Modells nicht überzuinterpretieren. Sie weisen darauf hin, dass die tatsächlichen Infektionsrisiken nur mit zusätzlichen experimentellen Daten bestätigt werden können.
Fußnoten
- Die physiologische Funktion von ACE2 besteht im Abbau des Blutdruck-steigernden Hormons Angiotensin II. Wenn SARS-CoV-2 mit seinem Spike-Protein an ACE2 bindet, kann dieser Abbau nicht erfolgen, und es kommt zu einem Überschuss an Angiotensin II. Das könnte erklären, warum insbesondere Patienten mit Herz-Kreislauf-Erkrankungen, Diabetes und Bluthochdruck oft schwer an COVID-19 erkranken.
Weiterführende Literatur
[1]. Lan, J., Ge, J., Yu, J., Shan, S., Zhou, H., Shilong, F., Zhang, Qi, Shi, X., Wang, Q., zhang, L., Wang X. (2020) Structure of the SARS-CoV-2 spike receptor-binding domain bound to the ACE2 receptor. Nature 581, 215–220.
[2]. Joana Damas, Graham M. Hughes, Kathleen C. Keough, Corrie A. Painter, Nicole S. Persky, Marco Corbo, Michael Hiller, Klaus-Peter Koepfli, Andreas R. Pfenning, Huabin Zhao, Diane P. Genereux, Ross Swofford, Katherine S. Pollard, Oliver A. Ryder, Martin T. Nweeia, Kerstin Lindblad-Toh, Emma C. Teeling, Elinor K. Karlsson, Harris A. Lewin. Broad host range of SARS-CoV-2 predicted by comparative and structural analysis of ACE2 in vertebrates. (2020) Proceedings of the National Academy of Sciences; DOI: 10.1073/pnas.2010146117


Der Zwischenwirt war ein Labor in Wuhan.
Und woher weiß Markweger das?
Er weiß es natürlich nicht, sondern trötet sein übliches von rechtsextremen Facebookseiten übernommenes Verschwörungsgewäsch hinaus.
Und was haben Sie zum Thema zu sagen ?
Die Suche nach einem Zwischenwirt für das SARS-CoV-2-Virus finde ich insoferne auch sehr interessant, weil in der Infektionskette zweifellos viele „Komponenten“ besonders auch Mikroben beteiligt sein könnten, eigentlich sein müssten.
Es geht nicht nur um den „Kampf“ Immunsystem – Viren, es gibt Fälle in denen Bakterien (abschwächend oder verstärkend) in das ohnehin schon sehr komplexe Geschehen eingebunden sind.
Mich würde es interessieren, ob es dazu systematische Forschungen, besonders im Zusammenhang mit SARS-CoV-2 gibt?
Meinst du ein Bakterium könnte als Überträger (Vektor) für das Coronavirus dienen? Davon habe ich bei den Coronaviren bisher noch nicht gehört.
@ Dramiga 24.09.2020, 07:25 Uhr
Über Wechsel- oder Vektorwirkungen im Zusammenhang mit Coronaviren habe ich auch nicht gehört, aber darüber dass Verstärkungseffekte bei Polioviren um das 500-Fache (Zitat 1) und darüber dass Lipopolysaccharide die Virenvermehrung und Infektion fördern können (Zitat 2), habe ich gelesen.
Es wäre insofern interessant, weil Corona eher Männer schwer schädigt, aber weniger Frauen und Kinder. Und da wiederum könnte die Ernährung die auf die Bakterienfauna einwirkt eine Rolle spielen, z.B. der Biergenuss in Ischgl beim Apres Ski.
Zitat scinexx:
1.) „Darmbakterien vervielfachen Infektiosität der Viren
In einer zweiten Studie beobachteten Forscher um Sharon Kuss von der University of Texas in Dallas ebenfalls einen direkten Einfluss der Bakterien: In Anwesenheit von Mikroben erhöhte sich die Infektiosität von Polioviren um das 500-Fache, berichten sie.“
2.) „Zuckermoleküle auf der Bakterienhülle als Virenhelfer
Die Ergebnisse deuten darauf hin, dass Viren die Darmbakterien für ihre Vermehrung und Übertragung ausnutzen“, sagen die Forscher. Offenbar spielten bestimmte Mehrfachzucker auf der Zelloberfläche der Mikroben die entscheidende Rolle für diese helfende Wirkung. In Laborversuchen reichte bereits die Anwesenheit dieser sogenannten Lipopolysaccharide, um die Virenvermehrung und Infektion zu fördern.
Diese Erkenntnisse werfen ein neues Licht auf eine bisher unbekannte Rolle der Mikrobenfauna für Viruserkrankungen“, schreiben Kane und ihre Kollegen. Das eröffne auch neue Ansätze für die Vorbeugung von Virusinfektionen der Schleimhäute, für virusspezifische Impfungen und für Therapien. (Science, 2011; DOI: 10.1126/science.1211057; DOI: 10.1126/science.1210718)
(Science / dapd, 14.10.2011 – NPO) 14. Oktober 2011“
Eine kürzlich in Wuhan, China, durchgeführte Studie bestätigte einen Zusammenhang zwischen der Zusammensetzung der Darmbakterien und der Veranlagung gesunder Personen COVID-19 zu bekommen. Erhöhte Konzentrationen von Lactobacillus-Spezies korrelierten mit höheren Konzentrationen von entzündungshemmendem Interleukin-10 und verbesserter Krankheitsprognose; erhöhte Konzentrationen von proinflammatorischen Bakterienspezies, darunter Klebsiella, Streptokokken und Ruminokokkus gnavus, korrelierten mit erhöhten Konzentrationen von proinflammatorischen Zytokinen und verschlechterter Krankheitsprognose. Diese Spezies wurden zuvor in der proinflammatorischen Darmumgebung von Patienten gefunden, die an einer Reihe von Erkrankungen wie Diabetes, Fettleibigkeit, Reizdarmsyndrom (IBD) und Bluthochdruck litten. Die Forscher haben einen Preprint veröffentlicht, der noch nicht den peer review durchlaufen hat.
Gou W, Fu Y, Yue L, Chen G-D, Cai X, Shuai M, Xu F, Chen H, Zhu Y, Xiao M-L, Jiang Z, Miao Z, Xiao C, Shen B, Wu X, Zhao H, Ling W, Wang J, Chen Y-M, Guo T, Zheng J-S. 2020. Gut microbiota may underlie the predisposition of healthy individuals to COVID-19. medRxiv doi:10.1101/2020.04.22.20076091.