DNA-Vervielfältigung in der Küche?
BLOG: Bierologie

Nachdem jetzt hoffentlich ganz viele von euch in der Küche gestanden haben, um aus verschiedensten Lebensmitteln DNA zu isolieren, können wir ja nun zum nächsten Schritt kommen. So spannend es auch ist, wenn man den weißen DNA-Schleim in den Händen hält: Noch spannender ist es natürlich, wenn man zumindest Teile dieser DNA auch vervielfältigen und vielleicht gleich auch noch analysieren könnte. Von etwaigen, rechtlichen Einschränkungen ganz abgesehen, gibt es da immer noch das Problem, dass man die dafür nötigen Zutaten und technischen Geräte meist nicht direkt in der Küche rumstehen hat. Die Standardmethode zur Vervielfältigung von DNA-Stücken in biologischen Labors weltweit ist die Polymerase-Kettenreaktion, kurz PCR, für deren Entdeckung Kary Mullis 1993 den Nobelpreis in Chemie bekam. Dabei nutzt man das namensgebende Enzym Polymerase, welches in jeder Zelle dafür verwendet wird, um DNA zu kopieren.
Während an der DNA-Vervielfältigung innerhalb der Zellen jedoch noch jede Menge andere Enzyme beteiligt sind, nutzt man bei der PCR stattdessen einfach verschiedene Temperaturen aus. Dazu erstellt man zuerst einen Cocktail in dem sich neben der Ausgangs-DNA, die man z.B. aus seiner Frucht isoliert hat, Polymerase als Kopiermaschine, Nukleotide als Bausteine für die Kopien und 2 kurze DNA-Stücke, die sogenannten Primer, damit die Polymerase auch rausfindet, ab wo sie mit der Kopierreaktion anfangen soll. Und diese Mischung setzt man nun verschiedenen Temperaturen aus: Als erstes setzt man den Cocktail hohen Temperaturen aus, damit die doppelsträngige DNA sich in 2 Einzelstränge aufteilt. Wenn das geschafft ist, dann setzt man die Temperatur herunter, damit sich die beiden Primer an ihren Zielregionen anlagern können. Sobald das geschehen ist kann man die Temperatur wieder heraufsetzen, damit die Polymerase ihre Arbeit verrichten kann.
Mit jedem Zyklus aus Trennung, Anlagerung und eigentlicher Vervielfältigung verdoppelt sich, zumindest theoretisch, die Anzahl der DNA-Kopien aus der gewünschten Region. Normalerweise macht man so 30-40 dieser Zyklen, um ausreichend viele Kopien seiner Wunsch-DNA zu vervielfältigen. Und da die Polymerase, die z.B. wir selbst in uns tragen, normalerweise bei so hohen Temperaturen nicht überlebt, nutzt man spezielle Polymerasen aus hitzebeständigen Bakterien. Denn sonst müsste man in jedem Zyklus per Hand neue Polymerase hinzufügen. Und obwohl man diese Zyklen theoretisch auch auf dem heimischen Herd mit 3 Herdplatten und entsprechend vielen Wasserbädern durchspielen könnte, so will man das ja trotzdem nicht per Hand machen. Wer will schon gute 2 Stunden vor dem Herd stehen und kleine Plastik-Reaktionsgefässe alle 30 Sekunden aus dem einen Wasserbad ins nächste überführen?
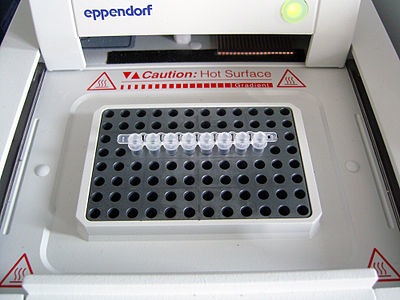
Deshalb gibt es dafür extra Geräte, dIe Thermocycler, in die man seine Proben einfach reinstellt und die genau diese Temperaturzyklen durchlaufen. Moderne Geräte machen dies dadurch, dass sie den Heizblock einfach sehr schnell hoch bzw. runterkühlen können. Ältere Geräte bestanden zum Teil aber auch einfach aus einem Roboterarm, der die Proben äquivalent zum Wasserbad in die verschieden vorgeheizten Platten gesteckt hat. Das ist bequem, allerdings für den Hobby-Anwender bislang nur beschränkt zugänglich: Denn die Dinger kosten normalerweise richtig viel Geld. Selbst bei eBay gehen Thermocycler gebraucht für bis zu 4000 US Dollar über die virtuelle Ladentheke (Für den Preis kriegt man auch schon gebrauchte DNA-Sequencer). Und selbst wenn man irgendwo ein Schnäppchen geschossen kriegt, dann hat man immer noch ein patentbehaftetes, geschlossenes System vor sich. Nicht unbedingt das, was man als Hobby-Bastler haben möchte.

Dem stellt sich das OpenPCR-Projekt entgegen. Für „nur“ 512 US Dollar kann man bei ihnen jetzt einen relativ einfachen Thermocycler als Bausatz kaufen. Der fertig zusammengeschraubte Thermocycler kann 16 Proben gleichzeitig verarbeiten und lässt sich über einen USB-Anschluss bequem mit einem Computer verbinden. Das ist schon ziemlich cool und vergleichsweise günstig. Aber um dem Projektnamen alle Ehre zu machen bleibt es nicht dabei, dass man das Ding selbst zusammenschrauben und auch wieder auseinandernehmen kann. Die gesamte Software, die den Cycler bedient ist, genauso Open Source, wie die Schaltpläne und die 3D-Files der Bauteile. Falls ihr also Ideen habt, wie ihr die Software oder die Hardware verbessern könnt, dann könnt ihr direkt selbst mit den Rohdaten rumspielen und es ausbessern.

Und auch für die weitere Analyse eurer vervielfältigten DNA gibt es mittlerweile Open Source-Lösungen. Denn die Vervielfältigung alleine ist ja nur der erste Schritt, zum sichtbar machen des Erfolgs nutzt man in der Regel die Gelelektrophorese. Dabei trägt man die Produkte seiner PCR auf ein Gel auf und legt Spannung an. Je nach Größe der Produkte können diese schneller oder langsamer durch das Gel wandern. Die im Gel aufgetrennten Produkte kann man dann durch eine UV-Sensitive Färbung nachweisen. Dank des Open Gel Box-Projekts gibt es aber auch da Abhilfe. Für 189 US Dollar gibt es einen einfachen Bausatz für eine Gel-Kammer. Und auch hier sind die Hardware-3D-Daten komplett veröffentlicht, so das man selbst Verbesserungen daran vornehmen kann.

Und mit der Kombination aus PCR und Elektrophorese kann man auch schon wirklich sinnvolle Analysen durchführen: Zum Beispiel schauen wie viele Short Tandem Repeats man so in seinem eigenen Genom an einer Stelle X trägt. Das sind kurze Sequenz-Fragmente die in unterschiedlicher Länge wiederholt werten, so ist zum Beispiel die Sequenz AGAGAGAGAGAGAG ein 7x wiederholter Tandemrepeat des Musters AG. Die Anzahl der Repeats bestimmt also die Länge des PCR-Produkts und damit auch wie schnell/weit das Produkt auf dem Gel in einer bestimmten Zeit läuft. Damit kann man dann also vom dem Gelbild Rückschlüsse auf die Anzahl der Repeats führen. Das ist zum Beispiel eine Methode, die man bei dem genetischen Fingerabdruck nutzt. Denn wenn man an genug Stellen die Repeats betrachtet, dann man ein Gesamtbild, dass statistisch nur sehr unwahrscheinlich ein zweites Mal vorkommen wird.
Falls ihr jetzt also Lust habt weiter mit DNA rumzuspielen, dann viel Spaß. Mit den hier vorgestellten, freien Methoden kann man schon viel Spaß haben. Und Open Source DNA-Sequencer werden bestimmt auch irgendwann bezahlbar.
Fotos: Eppendorf Cycler: Public Domain | OpenPCR-Cycler: OpenPCR-Project | Open Gel Box: pearl biotech


Bin letztens per Zufall über die OpenPCR auf Facebook gestolpert und fand das Gerät auf Anhieb cool. Mal schauen, wann ich mir zu Hause mein privates Labor einrichte ^^
In den USA ist diese ganze DIY-Geschichte ja schon ordentlich am laufen (im Vergleich zu hier) und wird ordentlich durch Andrew Hessel unterstützt. Insgesamt bin ich der Meinung, dass DIY-Biology erst durch das Aufkommen der synthetischen Biologie ins “Rollen” kam. Wie siehst du das?
Also ich hätte auch definitiv Lust, mir ein eines Lab in der Küche einzurichten. Allerdings ist das für mich alles noch relativ langweilig, solange es keinen OS-Sequencer gibt um über das Gel hinaus was rausfinden zu können. (Wobei mich ein bisschen Gentechnik mit Baktis auch reizen würde ;)).
Ich glaube auch, dass synthetische Biologie, gerade die BioBricks, der gesamten Bewegung einen guten Schub gegeben hab. Allerdings teilt sich das meinem Einblick nach dann doch auf. Es gibt die Leute die an Synth. Biologie interessiert sind und gern an Baktis rumspielen und da neue Funktionen einbauen wollen. Andere wollen mit PCR, Gelen & Co Grundlagenforschung betreiben bzw. Medizinische Forschung betreiben.
Hättest du denn an einem DIYBio-Lab à la Hackerspace denn Interesse?
Durchaus! Es stellt sich bloß die Frage, ob man wirklich Zeit neben der Tätigkeit als Diplomand/Doktorand/Postdoc hat mit solchen “Gimmicks” Wissenschaft zu betreiben. Das mag zwar interessant und auch cool sein, wenn man Experimente á la iGem machen möchte, für “intensive” Forschung muss man allerdings immer noch in ein “echtes” Labor. Du hast den Unterscheid ja schon angesprochen. Na gut, mit der DIY-Bio steht man ja erst am Anfang, wer weiss, was sich da die nächten Jahre entwickelt und wie schnell die Gerätepreise fallen bis man sich einen echten Sequenzierer und Co. für private Zwecke besorgen kann. Ich warte das mal ab und schaue mir an, was die Biohacker so in den USA treiben.
Ob man wirklich ein „echtes“ Labor benötigt um intensive/echte Forschung zu betreiben würde ich wirklich mal dahin gestellt lassen. Das kommt vermutlich auch stark darauf an, was man machen will.
Das sich nicht jeder in der Garage einen Not-So-LHC hinstellen kann ist vermutlich klar. Aber mit einer Tischzentrifuge, einem Cycler und einer Gelkammer und eventuell einem Sequencer kommt man doch auch schon relativ weit. Und wer es weniger feucht mag, der findet in den Repositories doch schon Unmengen an biologischen Daten auswerten kann und auch mit in seine Experimente einbeziehen kann.
Ich würde das deshalb gar nicht mal als reine Spielerei abtun wollen. Allerdings ist die dafür nötige Freizeit dann wohl das eigentliche Problem. Aber andererseits kann man als PhD-Student/Postdoc seine Arbeit dann auch wortwörtlich mit nach Hause nehmen 😉
Die Frage ist, ob man das wirklich möchte? Ich irgendwie nicht, da man seine Freizeit doch auch mal für andere Dinge nutzen sollte. Naja, leichter gesagt als getan. Wer im Labor arbeitet, hat oft nicht den Luxus einer gediegenen Freizeit. So bekomme ich es zuminest aus meinem Umfeld mit.
Also ich nehme meine Arbeit gerne mit nach Hause. Das hat den Vorteil, dass ich da relativ ungestört bin, die Musik meiner Wahl hören kann und mir die Zeit da relativ frei einteilen kann. Da arbeite ich dann lieber mal bis spät in die Nacht und Schlaf dafür aus 😉
Primer
Vielen Dank für diese äußerst spannenden DNA-Bastelbeiträge!
Salz, Spüli und Schnaps habe ich im Supermarkt bekommen. Die Extraktion kann also schon losgehen.
Aber in welcher Abteilung finde ich Taq-Polymerase und Nukleotide? Vor allem: woher weiß ich, welchen Schnipsel der DNS ich kopieren will und woher nehme ich dann die passenden Primer?
Für die Nukleotide, Primer und Taq muss man dann leider doch wieder in den Online-Versandhandel wechseln, z.b. zu Genecraft. Und die entsprechenden Primer kann man sich entweder selbst designen oder schauen ob man per Google schon fertige Primer-Sequenzen für das Gen das einen interessiert findet.