Nanocillus – `cause spore is more!
BLOG: SignalBlog

Patienten, die unter chronisch entzündlichen Darmerkrankungen wie z.B. Colitis ulcerosa leiden, sind auf lebenslange medikamentöse Therapien angewiesen, um die inflammatorischen Prozesse im Körper unter Kontrolle zu halten. Systemische Nebenwirkungen von Kopfschmerzen bis hin zu lebensgefährlicher Blutarmut schrecken viele Menschen davon ab, Medikamente täglich und regelmäßig einzunehmen. Dies ist allerdings für den Erfolg der Therapie essentiell. Deutschlandweit sind mehr als 120.000 Menschen von Colitis ulcerosa betroffen. Die Diagnose wird meist in jungen Jahren, im Alter von 30 und 40, gestellt.
Wir, das diesjährige iGEM (international Genetically Engineered Machine) Team der Universität Freiburg, haben es uns zum Ziel gesetzt, mit einer neuen Form der gezielten Medikamentenapplikation („targeted drug delivery“) mit Sporen des Bakteriums B. subtilis die Therapie von Colitis ulcerosa zu reformieren, und damit an die Erfolge der vorherigen Freiburger iGEM Teams anzuknüpfen.
Auch dieses Jahr besteht das iGEM Team aus einer interdisziplinären Mischung. Der Mix aus Biologie, Biochemie, -physik, Chemie, Informatik und Medizin ermöglicht es uns, unser Projekt aus verschiedenen Blickwinkeln zu betrachten und das Thema effektiver anzugehen.
Nach wochenlanger Einarbeitung und ausgiebigem Brainstorming sind wir zu dem Entschluss gekommen, Medikamente mithilfe von sporengebundenen Enzymen lokal und gezielt aktivieren zu lassen. An der Sporenoberfläche sind Nanoantikörper gebunden, die bestimmte Strukturen erkennen und spezifisch binden.
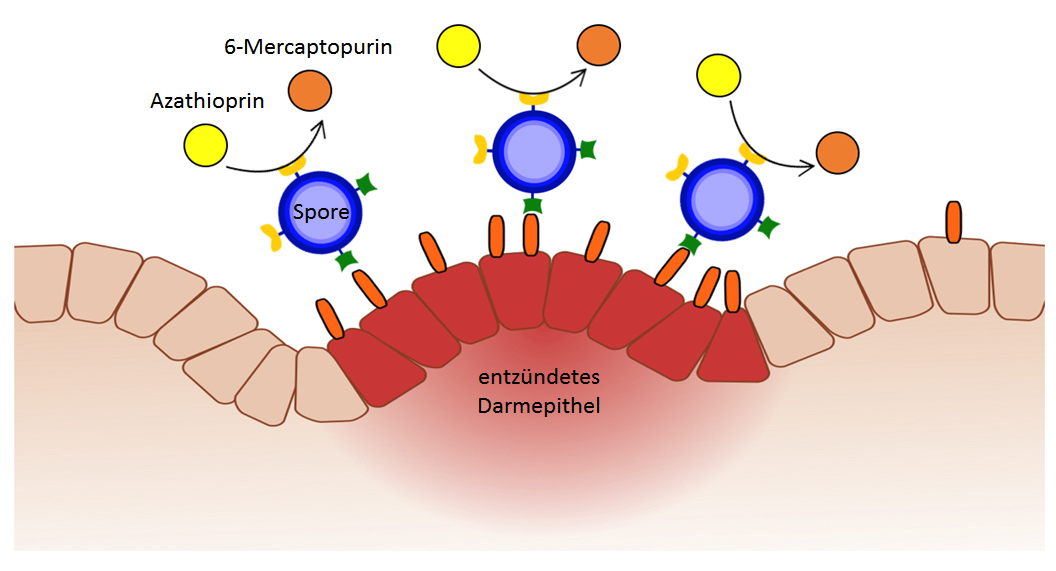
Als Paradebeispiel eignet sich das immunsupressive Medikament Azathioprin, das in der Erhaltungstherapie von Colitis ulcerosa verwendet wird. Das Enzym Gluthation-S-Transferase aktiviert Azathioprin zu 6-Mercaptopurin, welches antientzündlich wirkt.
Sporen, die einerseits Nanoantikörper gegen CEA (carcinoembryonic antigen) auf ihrer Oberfläche exprimieren und folglich spezifisch an entzündete Dickdarmepithelzellen binden, gleichzeitig aber auch das Enzym Gluthation-S-Transferase tragen, können das im Darmlumen vorhandene Azathioprin gezielt aktivieren. (Bild 1)
Dieses Prinzip lässt sich natürlich auch auf andere Medikamente anwenden, die von Enzymen aktiviert werden.
Da es sich bei den B. subtilis Sporen um einen genetisch modifizierten Organismus handelt, werden verschiedene Mechanismen, wie etwa „Germination Knockout“ und ein „Kill Switch“ eingebaut. Dies verhindert, dass die Sporen auskeimen können und sorgt dafür, dass sie sich beim Auskeimen selbst neutralisieren. Sollten beide Mechanismen versagen, würden die Keime die genetische Veränderung nach ein paar Generationen verlieren, da sie ihnen keinen evolutionären Vorteil verschafft. Auf Grund dieser drei Mechanismen sehen wir kein Risiko für Mensch und Umwelt, sondern eine Chance das Leben vieler Patienten einfacher zu machen, indem wir ihnen unangenehme Nebenwirkungen ersparen.
Ein zusätzlicher Vorteil unseres Systems liegt in der günstigen Produktion der Sporen und deren Stabilität gegenüber Umweltfaktoren wie Temperatur, Feuchtigkeit und Licht, sodass diese unkompliziert gelagert und aufbewahrt werden können.


Gute und sehr allgemein anwendbare Idee. Allerdings werden Patienten, die heute an einer Colitis ulcerosa leiden wohl erst in 10 bis 20 Jahren in den Genuss einer solchen Therapie kommen, denn solange muss man schon rechnen von der Idee bis zum Einsatz am Menschen. Zuerst wird dieses neue Applikationsverfahren wohl an (humanisierten) Mousemodellen für Colitis ulcerosa getestet werden müssen, später folgen klinische Studien. Eine Abkürzung des Verfahrens bei durchschlagendem Erfolg ist aber denkbar.