Die großen Fragen – Werden wir die Alterung besiegen?
BLOG: 1ife5cience

 Dieser Blogbeitrag ist Teil des Bloggewitters zum Liveblog “Die großen Fragen an die Wissenschaft” bei Zeitonline.
Dieser Blogbeitrag ist Teil des Bloggewitters zum Liveblog “Die großen Fragen an die Wissenschaft” bei Zeitonline.
Der sagenumwogene Jungbrunnen steht, will man der Werbung glauben, in der Drogerie und ist dort für teures Geld zu erwerben. Oder aber man folgt Gurus, die einem erklären, wie man sich ernähren soll, am besten mit Produkten an denen sie selbst verdienen. Oder aber, man schaut sich die Wissenschaft an.
Es gibt durchaus Möglichkeiten, sein Leben zu verlängern. Wie ich ja schon einmal beschrieb, ist DNA-Schaden eine wichtiger Faktor in der Alterung. Also sollte man alles meiden, was einem unnötigerweise DNA-Schäden aussetzt. So zum Beispiel Schadstoffen wie sie in Tabakrauch sind. Außerdem sollte man Strahlenexposition vermeiden – ob nun durch die Sonne oder einen Nuklearbrennstab. Gegen Sonne hilft ein Lichtschutzfaktor und Nichtrauchen ist günstiger und hält gesund. Gegen Radioaktivität hilft nicht viel, außer man will den Rest seines Lebens im Atombunker leben.
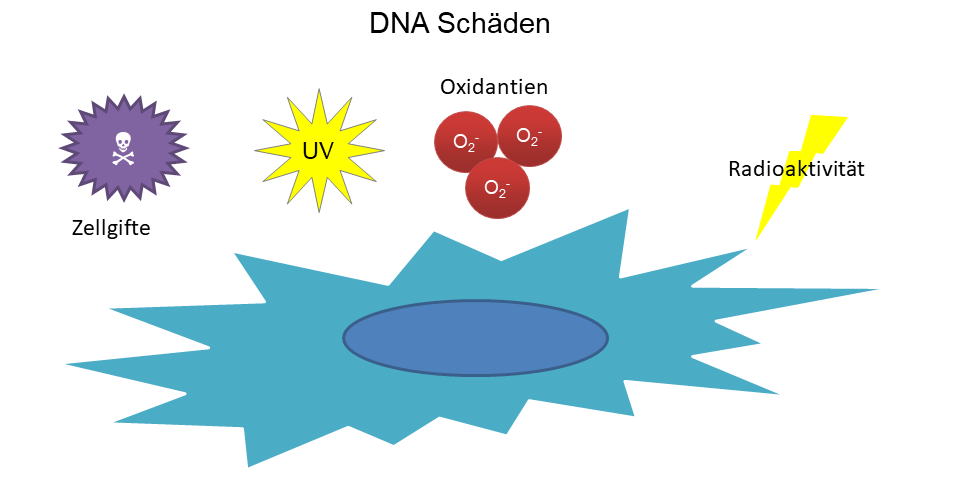
Wie genau DNA-Schaden die Alterung begünstigt habe ich schon einmal beschrieben. In der Kurzfassung: Die sich in unserer DNA angesammelten Schäden können irgendwann dazu führen, dass unsere Zellen sich aufhören zu teilen. Sie werden „seneszent“, was eigentlich nichts anderes heißt als „gealtert“. Seneszente Zellen sind erst einmal dafür da, das Gewebe aufrecht zu erhalten, denn würde die Zelle direkt sterben, also Apoptose begehen, wäre ja eine Lücke zu füllen. Gleichzeitig signalisieren die Zellen ihren Nachbarzellen, dass ein Problem besteht. Sie schütten Entzündungsstoffe aus. Diese seneszenten Zellen werden normalerweise vom Immunsystem abgebaut. Mit dem Alter funktioniert das aber nicht mehr so gut. Entweder das Immunsystem wird schwächer oder es entstehen zu viele neue Zellen. Oder beides.
Die von den seneszenten Zellen ausgeschütteten Entzündungsstoffe nennt man auch „Senescence Associated Secretory Phenotype“ oder SASP. Der SASP sorgt für eine andauernde Entzündung, die das Gewebe um die seneszente Zelle herum verändert. Unter anderem kann der SASP auch andere Zellen in die Seneszenz führen. Außerdem können Entzündungsstoffe schon vorhandene Krebszellen zum Wachstum anregen. Krebs und Seneszenz der Zelle sind beide Folge des DNA-Schadens, deswegen ist es wahrscheinlich, dass beides miteinander einhergeht. Tatsächlich findet man in bösartigen aber auch gutartigen Tumoren seneszente Zellen. Je nach Setting scheinen seneszente Zellen sich hier unterschiedlich zu verhalten.

Wenn man die Alterung aufhalten möchte, dann ist die logischste Möglichkeit, die seneszenten Zellen, die entstehen zu verringern, also, den DNA-Schaden zu minimieren. Oben habe ich schon sehr einfache Möglichkeiten genannt. Leider entsteht DNA-Schaden aber auch einfach so. Durch unsere Atmung etwa, oder die Nahrungsaufnahme. Die entstehende Energie setzt sogenannte Sauerstoffradikale frei, die unsere DNA kaputt machen können.
Um diese Sauerstoffradikale zu reduzieren versuchen es einige Menschen mit „Kalorischer Restriktion“. Wenn man weniger isst, kann der Körper auch weniger Sauerstoffradikale bilden. Ein weiterer Vorteil ist, dass hungernde Zellen einige Schutzmechanismen haben, die in erster Linie vor Krebs schützen können. Leider ist das nur eine Seite der Medaille, denn der durch kalorische Restriktion aktivierte Signalweg, die Autophagie, bedeutet, dass Zellen beginnen, sich selbst zu „essen“ um am Leben zu bleiben. Es werden also Überlebenssignale ausgesendet, die auch Krebszellen wachsen lassen können. Außerdem ist Hungern auch nicht sonderlich angenehm. Man ist müde, friert schneller und ist auch anfälliger für Krankheiten.
Eine weitere Möglichkeit ist, seneszente Zellen künstlich abzubauen. Hier hatte man zunächst begonnen, Mäuse mit Progerie, also verfrühter Alterung, genetische so zu verändern, dass ihre Zellen nicht mehr in Seneszenz gehen konnten. Mäuse mit dieser genetischen Veränderung zeigten deutlich weniger Alterserscheinungen als ihre Geschwister – sie wurden jedoch gleich alt.
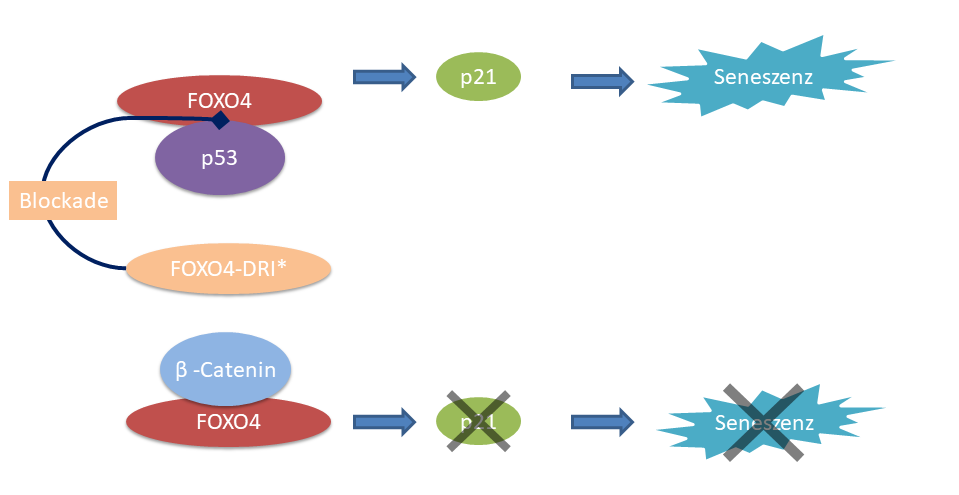
Prinzpiell wäre es also möglich, uns gesünder „alt“ werden zu lassen. Nun müsste man jedoch etwas finden, mit dem man seneszente Zellen gezielt entfernen kann. Eine Möglichkeit ist zum Beispiel FOXO4. FOXO4 ist eigentlich ein Transkriptionsfaktor, also ein Protein, welches die Abschrift von Genen bewirkt. So werden neue Proteine gebaut. FOXO4 führt durch seine Interaktion mit p53 dazu, dass Zellen eher in Seneszenz gehen. p53 ist ebenfalls ein Transkriptionsfaktor, der sowohl Apoptose als auch Seneszenz bewirken kann. FOXO4 kann aber diese Vorgänge auch unterdrücken. FOXO 4 kann über das Molekül β-Catenin das Seneszenz-Molekül p21 bremsen. Daraus folgt, um die Entstehung seneszenter Zellen aufzuhalten, müssten wir dafür Sorgen das FOXO4 weniger mit p53 und mehr mit β-Catenin spielt. Das könnte man vor allem mit peptiden, also Miniproteinen erreichen, die in die Zellen eindringen können und in den Signalweg eingreifen. Dies müsste jedoch hochspezifisch sein. Allererste Schritte konnten mit einer Art FOXO4-Isomer erzielt werden. Dadurch wurde die Bindung von FOXO4 zu p53 unterbrochen und p53 löste über die Zerstörung der Mitochondrien den Zellselbstmord aus.
Eine weitere Möglichkeit konnte man in Mäusen aufzeigen. Mit den niedermolekularen Inhibitoren Dasatinib und Quercetin konnten bereits seneszente Zellen getötet werden. Leider sind beide Substanzen nicht spezifisch. Da Dasatinib ein Krebsmedikament nicht ohne Nebenwirkungen ist, wäre es auch schwierig dieses beim Menschen anzuwenden.
Hoffnungen setzt man auch in die Hemmung der BCL-Proteinfamilie. So konnten ebenfalls seneszente Zellen abgetötet werden. Leider sind BCL-Proteine sehr häufig in Zellen vertreten und auch wichtig für den programmierten Zelltod, eine wichtige Barriere gegen Krebs.


Jedenfalls sind wir bezüglich seneszente Zellen nicht mehr im reinen Forschungsstadium. Es gibt mehr und mehr Firmengründen im Bereich Senolytika (Entfernung von seneszenten Zellen) und auch die Erforscher der FOXO4-p53 Interaktion haben nun ein modifiziertes Peptid geschaffen, welches seneszente Zellen in den Tod treibt. „Mouse Work is over“ sagen diese Forscher, klinische Studien bald schon am Menschen stehen bevor.
Ältere senolytische Techniken benutzt Unity Biotechnology und diese stehen kurz vor klinischen Tests. Ausgeklügeltere Herangehensweisen mit Plasmiden und synthetischer Biologie findet sich bei den Firmen Oisin und CellAge. Bei der Vielzahl von Firmengründungen, die es im Bereich Senolytika schon gibt und den ganz unterschiedlichen Ansatzpunkten, darf man damit rechnen, dass Medikamente oder Therapien, die bei den seneszenten Zellen ansetzen, in den nächsten 10 in die klinische Praxis übergehen und da ja über 90% aller Menschen ein Alter erreichen, in denen seneszente Zellen zum Problem werden, könnten Senolytica zu den am meisten verkauften Medikamenten überhaupt werden.
Und die Leser dieses Blogs dürfen sogar hoffen, dass sie selbst noch von Senolytica profitieren – falls sie noch 10 bis 20 Jahre durchhalten.
Ich glaube das die Suche gar nicht einmal der Unsterblichkeit ansich gilt. Vielmehr geht es bei dieser Frage doch immer darum die Alterung zu verhindern. Auch wenn es etwas widersprüchlich klingen mag, gerade in der heutigen Zeit wird ja gut sichtbar es geht nicht darum alt zu sein oder zu werden sondern um den Weg dahin. Das altern ansich ist hier doch zumeist das zu bekämpfende Feindbild. Dementsprechend wird ja auch immer von der ewigen Jugend gesprochen, vom Jungbrunnen etc. es geht primär nicht darum unsterblich zu werden, sondern darum Jung zu bleiben. Und die Unsterblichkeit ist davon quasi nur die Logische überlegung das wenn man jung bleibt wohl unsterblich wäre…
Ja, alt werden bedeutet meist – oder eigentlich immer? – krank werden. Und jede chronische Krankheit führt irgendwann zum Tod.
Der “Jungbrunnen” steht in Bad Harzburg.
Besonders gefällt mir die alte Frau, die nicht selbst hineinsteigt, sondern den Schwanz ihres alten Katers eindippt. „Honi soit qui mal y pense“
https://www.tripadvisor.com/LocationPhotoDirectLink-g198583-d629964-i193107056-Der_Jungbrunnen-Bad_Harzburg_Lower_Saxony.html
http://www.bad-harzburg.de/freizeit-kultur/bad-harzburg/jungbrunnen.html
HSP90-Inhibitoren (HSP=heat shock protein) scheinen wirksam zu sein sowohl gegen seneszente als auch gegen Krebszellen und versprechen damit, als Senolytica auch antikanzerogen zu wirken! Zitat (von DeepL übersetzt, unverändert übernommen):
Der Tod steckt im Darm , sagt ein Sprichwort, deshalb sollte man bei der Diskussion auf die Ernährung achten.
Stetiger Fischverkehr verlängert das Leben. An apple each day keeps the doctor away. Es gibt unzählige solcher Sprichwörter. Sogar die Wirkung von Knoblauch gegen Vampire wird nicht vergessen.
Man sollte mal diese Tatsachen wieder in den Focus nehmen.
wird vom physorg-Artikel It’s mathematically impossible to beat aging, scientists say negativ beantwortet, letztlich weil (Zitat)
Diese Aussagen sind eine Zusammenfassung des PNAS-Artikels Intercellular competition and the inevitability of multicellular aging. Im Abstract wird die gängige Theorie, warum es überhaupt Alterungsvorgänge gibt – nämlich weil die Evolution Altern begünstige, indem ungünstige Genkonstellationen, die sich erst später im Leben auswirken, nicht wegselektiert würden – in Frage gestellt und behauptet, multizelluläres Leben sei ohne Alterung nicht möglich. Dies ergebe ihr Modell des Zusammenspiels von interzellulälerem Wettbewerb, Altern und Krebs. Insbesondere geht ihr Modell davon aus, dass nicht alle Zellen eines Organismus jederzeit miteinander kooperieren müssen. Zudem ist mit einer Beschleunigung des Alterungsvorgangs zu rechnen, wenn die Reparaturmechanismen selbst altern.
Das vorgestellte Modell ist vor allem ein mathematisches Systemmodell. Es scheint mir allerdings nicht zu berücksichtigen und zu erklären, dass bestimmte Quallen (Turritopsis dohrnii) tatsächlich eine ewig währende Regeneration zeigen. Allerdings ist die ewig währende Lebensdauer von Turritopsis dohrnii gerade dadurch gekennzeichnet, dass sich der ewig lebende Teil dieses Organismus wieder zurückentwickelt (wieder verjüngt), bevor es den nächsten Lebenszyklus beginnt (Zitat Wikipedia):
Fazit: Wenn man einen Organismus als (mehr oder weniger) freiwilliges Zusammenspiel von Zellen betrachtet, dann ist es tatsächlich schwierig vorstellbar, dass dieses Zusammenspiel auf ewige Zeit funktionieren soll – vor allem darum, weil es für gewisse Veränderungen keinen garantierten Rückstellmechanismus gibt, der den “gesunden” Zustand wiederherstellt, denn jeder Rückstellmechanismus (Reperaturmechanismus) kann selber einer unkontrollierten Veränderung unterworfen sein.
Meine eigene Folgerung: Die Natur selbst kann Altern wohl nicht völlig verhindern. Aber wenn der Mensch nachhilft, dann kann der Alterungsprozess möglicherweise x-Mal gestoppt und gar rückgängig gemacht werden. Wenn wir das Altern also mit medizinischen Mitteln stoppen oder rückgängig machen können, dann werden wir diesen Eingriff immer wieder wiederholen müssen.
Antikörper gegen seneszente Zellen und gentherapiebasierte Verfahren zur Elimination von seneszenten Zellen sind zwei neue Methoden, erforscht von:
– Siwa Therapeutics erforscht Antikörper gegen seneszente Zellen
– Oisin Biotechnologies eliminiert seneszente Zellen über einen Angriff auf Zellen, die p16 exprimieren indem in diesen Zellen ein Gen über eine Fähre (Liposom) eingeschleusst wird, welches schliesslich die seneszenten Zellen absterben lässt.
Beide Firmen berichten zudem, dass ihr Ansatz auch gegen Krebszellen wirkt. Im Falle von Siwatherapeutics stoppten die Antikörper gegen seneszente Zellen auch die Metastasierung eines Brustkrebskarzinoms. Oisin Biotechnologies dagegen hat zur Krebsbekämpung ein anderes Ziel als p16 gewählt, nämlich p53 und konnte damit ein metastasierendes Melanom gewichtsmässig um das Zwanzigfache verkleinern.
Quercetin ist das einzige (schwache) Senolytica, welches heute schon empfohlen werden kann, denn es kommt in Äpfeln und Bromelain (aus Ananas gewonnenes Enzym) vor und hat folgende Wirkungen (Achtung gemäss GarmaOnHealth.com, übersetzt von DeepL): Senkt das Entzündungsniveau, Bekämpft Allergien, Unterstützt die Gesundheit des Herzens, Hilft bei der Schmerzbekämpfung, Könnte Ausdauer fördern, Könnte helfen, Krebs zu bekämpfen, Hilft, die Gesundheit der Haut zu schützen.
Negative Nebenwirkungen sind nicht bekannt.
Ergänzung: Über Quercetin liest man in der Wikipedia:
500 mg Quercetin pro Tag sollte man schon einnehmen, also 8 Kilogramm Brokkoli pro Tag oder (mindestens) 1 Kilogramm Äpfel oder 300 Gramm Kaper oder ebensoviel Liebstöckel oder mehrere Aussenringe von Zwiebeln.
Nun, vielleicht ist die Mittelmeerküche ja auch so gesund, weil viele Gerichte Kapern enthalten (z.B. Vitello tonnato, Spaghetti alla puttanesca,). Wer weiss?
Ein schöner, zum Nachdenken anregender Artikel.
@Robert .. sicher spielt die Ernährung und ein intaktes Verdauungssystem eine bedeutende Rolle beim Alterungsprozess, ohne Zweifel, aber auch andere Dinge, die zum Beispiel das Altern in unserer Schaltzentrale (Gehirn) nachweislich beeinflussen, sind bedeutend.
Ich denke da auch an Alkohol, Bewegungsarmut oder das Rauchen.
Seit 2015 ist bekannt, dass Altern ein epigentisch regulierendes artenübergreifend identisches Programm mit unterschiedlichem Geschwindigkeitsablauf ist. Drei Jahre sind notwendig gewesen, das regulierende Gennetzwerk ausfindig zu machen. Seit 2018 ist ein Startup an der Entwicklung einer “Therapie” mit kurzlebigen Modellorganismen unterwegs. Altern ist ein gewollter Prozess der Natur, um unsere individuelle DNA Konfiguration an den Umweltbedingungen zu testen und uns zur geschlechtlichen Rekombination zu zwingen, wenn diese Konfiguration erfolgreich ist. Wir sind jetzt höchstens nur ein besonderer Zweig des Lebens, da wir mit allen Zellen näher oder ferner verwandt sind. Unsere zukünftige Technologie besitzt die Fähigkeit uns und das Leben allgemein auf der evolutionären Reise in einem Sprung zu beschleunigen.
Unabhängig von den sich anhäufenden seneszenten Zellen, ändert/verschlechtert sich auch der Stoffwechsel und vieles mehr, z.B. die Zusammensetzung des Blutes. Bereits gezeigt wurde, dass die Infusion von „jungem Blut“ Alterungsprozesse vorübergehend reduziert. Neu konnte gezeigt werden, dass die Entfernung der meisten Stoffe im Blutserum den gleichen Effekt hat. Mit andern Worten: das eigene Blut 🩸 macht einen alt und ein Ersatz des eigenen Serums durch neutrales Serum verjüngt einen wieder. Siege dazu: Diluting blood plasma rejuvenates tissue, reverses aging in mice