Wächter des Gehirns – kleine Zellen mit großer Wirkung
BLOG: KlarText Blog

Für seine Bewerbung um den KlarText-Preis hat der Biologe Peter Wieghofer erklärt, was er in seiner Doktorarbeit erforscht hat.
Alltäglich stehen wir einer Armada von Krankheitserregern gegenüber, die unser Immunsystem auf Trab halten. Das Gehirn besitzt eine ganz eigene Abwehrstrategie, die weit mehr kann als Keime abzutöten. Als zentrale Schaltstation sämtlicher lebenswichtiger Vorgänge, wie Atmung und Nahrungsaufnahme, kommt dem Gehirn eine ganz besondere Bedeutung zu. Es gehört zu den komplexesten Strukturen, die die Natur bisher hervorgebracht hat. Störungen in seiner Funktion können ganz unterschiedlicher Art sein: Bei einem Schlaganfall treten sie akut auf, bei altersbedingten Veränderungen ist der Prozess schleichend. Das Gehirn bedarf daher eines besonderen Schutzes. Physikalisch ist dieser gegeben durch die Widerstandskraft des Schädels und durch die Hirnhäute, die das Nervengewebe sicher umschließen. Aufgrund des hohen Energie- und Sauerstoffverbrauches ist das Gehirn sehr dicht von speziellen Gefäßen durchzogen, die eine weitere einzigartige Schutzfunktion bilden: die Blut-Hirn-Schranke. Ohne diese Barriere könnten unterschiedlichste Stoffe, Krankheitserreger oder Zellen ungehindert aus dem Blut in das Gehirn eindringen.
Nicht nur die Funktions- und Schutzmechanismen spiegeln die Komplexität des Gehirns wider, sondern auch die Art und Zusammensetzung der Zellen, die am Aufbau des Gehirns beteiligt sind. Neben den Nervenzellen, den bekanntesten Vertretern, gibt es noch weitere Arten von Zellen, die im Besonderen strukturbildend und essentiell für die Nährstoffversorgung des Gehirns sind: die Gliazellen.”Glia” abgeleitet aus dem Griechischen bedeutet “Kitt” oder “Leim”. Daher wurden diese Zellen von dem deutschen Pathologen Rudolf Virchow im 19. Jahrhundert erstmals als “Nervenkitt” bezeichnet. Innerhalb der vielfältigen Gruppe der Gliazellen gibt es nur einen Zelltyp, der dem Immunsystem zuzuordnen ist: Die Mikroglia. Sie verdanken ihren Namen ihrem verhältnismäßig kleinem Zellkörper, und machen zudem den geringsten Anteil der Gliazellen aus.
Mikroglia: Wächter und Architekten
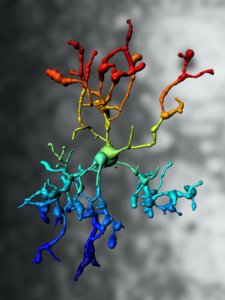
Mikroglia besitzen feinste Verästelungen, um kontinuierlich ihr Territorium abzutasten. Obwohl sie klein sind, gehören sie zu den Makrophagen, den großen Fresszellen. Wie Makrophagen in anderen Organen, wurden Mikroglia lange Zeit als die Wächter des Gehirns angesehen, die erst in Aktion treten, wenn akute Bedrohungen, beispielsweise durch eine Infektion, auftreten. Erst seit einigen Jahren versteht man, dass diese Zellen darüber hinaus nicht nur die Wächter, sondern auch die Architekten des Gehirns sind. Schon vor der Geburt beeinflussen Mikroglia die sich entwickelnden Nervenzellen und wie sich diese untereinander verknüpfen. Fehlen Mikroglia oder ist ihre Funktion beeinträchtigt, kann sich das Gehirn nicht richtig entwickeln.
Durch die nur schwach ausgeprägte Fähigkeit sich selbst zu erneuern, ermüden Mikroglia im Laufe des Lebens. Daher häufen sich Hinweise, dass Erkrankungen des Gehirns im hohen Alter, wie beispielsweise die Alzheimer- oder Parkinson-Erkrankung, durch Mikroglia ausgelöst oder zumindest beeinflusst werden. Doch auch bei jungen Erwachsenen, die an Multipler Sklerose (MS) leiden, sind Mikroglia an der für die Erkrankung typischen chronischen Entzündung des Gehirns beteiligt. Mikroglia erfüllen somit weitreichende Funktionen, die verdeutlichen wie wichtig diese lange unterschätzten Zellen für ein gesundes und funktionierendes zentrales Nervensystem sind. Krankhafte Mikroglia hingegen können erhebliche Schäden verursachen.
Ursprung von Makrophagen
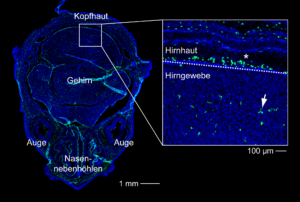
Neben dem Gehirn besiedeln Makrophagen auch Gehirn-assoziierte Gewebe, zu denen beispielsweise die Hirnhäute zählen sowie die Gefäße, die das Gehirn durchziehen und versorgen. Lange Zeit nahm man an, dass Mikroglia und Gehirn-assoziierte Makrophagen von Blutzellen abstammen. Diese Annahmen basieren überwiegend auf genetisch veränderten Mausmodellen, in denen weiße Blutkörperchen mit einem Farbstoff markiert wurden, um sie verfolgen zu können. Fand man eine markierte Zelle im Gehirn, war sie folglich aus dem Blut eingewandert. Allerdings musste man erst das körpereigene blutbildende System entfernen, um es durch das eines genetisch veränderten Spendertieres zu ersetzen. Die hierfür benötigte Bestrahlung tötet aber nicht nur das Knochenmark ab, sondern führt auch zu einem Zusammenbruch der so wichtigen Blut-Hirn-Schranke. Dadurch gelangten Zellen aus dem Blut in das Gehirn, die unter normalen Bedingungen am Einlass gehindert worden wären.
Diese lange unerkannte Nebenwirkung der Bestrahlung stellt letztlich die in der Vergangenheit gezogenen Schlussfolgerungen über den Ursprung der Mikroglia in Frage. Zu Beginn dieses Jahrzehnts identifizierten Wissenschaftler die tatsächliche Herkunft von Mikroglia. Während der Embryonalentwicklung im Mutterleib bilden sich unreife Makrophagen. Diese besiedeln Strukturen, aus denen im weiteren Verlauf das Gehirn entsteht, und reifen dort zu Mikroglia heran. Ein Umdenken in Bezug auf den tatsächlichen Ursprung von Mikroglia setzte ein.
Durch die Anwendung eines neuartigen Mausmodells führte ich dieses Umdenken weiter und konnte erstmals zeigen, dass nicht nur Mikroglia, sondern auch die Makrophagen in den Hirnhäuten eine von weißen Blutkörperchen unabhängige Gruppe von Immunzellen sind. Mit diesem Mausmodell ist es erstmals möglich, langlebige Makrophagen von den kurzlebigen weißen Blutkörperchen im Blut zu unterscheiden.
Die Ergebnisse bildeten die Grundlage für die Hypothese, dass Mikroglia und alle mit dem Gehirn assoziierten Makrophagen einen hohen Verwandtschaftsgrad besitzen und einen gemeinsamen Ursprung in der frühen Entwicklung haben. Diese Annahme stand im starken Gegensatz zu der existierenden Literatur, die bis in die 1980er Jahre zurückreicht. Mit Hilfe dieses neuen Mausmodells war es mir am Ende möglich, die Hypothese zu bestätigen und das Lehrbuchwissen der letzten 30 Jahre zur Diskussion zu stellen.
Anwendungsgebiete der Makrophagenforschung
Warum ist es wichtig, den Ursprung der Makrophagen im Gehirn zu kennen? Die Besiedelung des Gehirns in einer frühen Entwicklungsphase findet noch vor der Bildung der Blut-Hirn-Schranke statt. Die damit einhergehende Abschirmung der Mikroglia und ihren Verwandten vom Blut bedingt gleichzeitig die hohe Langlebigkeit dieser Zellen. Erst dadurch ist es möglich, das Gehirn durch die Blut-Hirn-Schranke nach außen abzuschirmen und gleichzeitig einen dauerhaften immunologischen Schutz zu gewährleisten. Allerdings sind dieser von der Natur verfolgten Strategie auch Grenzen gesetzt: Funktionieren Mikroglia nicht mehr richtig, sind Erkrankungen programmiert. Daher ist es umso wichtiger, diese Zellen in all ihren Ausprägungen zu charakterisieren. Ist der Ursprung eines bestimmten Zelltyps bekannt, lässt sich dessen Vorläufer, aus dem sich der Zelltyp entwickelt, unter Umständen im Reagenzglas erzeugen. Heutzutage ist man beispielsweise in der Lage, aus Zellen der Haut unterschiedlichste Arten von anderen Zelltypen zu bilden.
Gentechnische Methoden entwickeln sich rasant weiter und eröffnen die Möglichkeit, Zellen schnell, kostengünstig und effizient genetisch zu verändern. Dadurch ist es möglich, ein einzelnes defektes Gen zu reparieren oder zu ersetzen. Beispielsweise nach einem Transfer der körpereigenen, “reparierten” Immunzellen in den Patienten fanden diese ihren Weg ins Gehirn und ein dort vorherrschender Stoffwechseldefekt konnte behoben werden. Daran wird deutlich, wie das Immunsystem dazu genutzt werden kann, krankheitsbedingte Veränderungen im Gehirn zu korrigieren.
Bei einem vorsichtigen Blick in die Zukunft wäre auch ein Ersetzen der fehlgeleiteten Mikroglia mit weitreichenden Behandlungsoptionen für Erkrankungen des zentralen Nervensystems denkbar. Die Identifikation des Ursprungs der Makrophagen in den Hirnhäuten könnte in Zukunft auch hier neue therapeutische Wege aufzeigen.
Ein bedeutendes Anwendungsgebiet meiner Forschung ist die Behandlung von Multiple Sklerose (MS): Bei MS wurde nicht nur für Mikroglia im Gehirn, sondern auch für Makrophagen in den Hirnhäuten eine Beteiligung am Verlauf dieser Erkrankung nachgewiesen. Gewisse Aspekte der MS spiegeln sich im Mausmodell wider, so dass therapeutische Ansatzpunkte ausfindig gemacht werden können. In diesem Kontext konnte ich erstmals gezielt in Mikroglia und in mit dem Gehirn assoziierten Makrophagen einen Entzündungsfaktor ausschalten, wodurch die Mäuse keinerlei Symptome von MS mehr entwickelten. Wurde dieser Faktor hingegen in Nervenzellen und anderen Gliazellen unschädlich gemacht, zeigte sich keine Verbesserung der Symptomatik. Die Makrophagen sind den Nerven- und den weiteren Gliazellen in ihrer Anzahl stark unterlegen. Die Ergebnisse meiner Forschung belegen jedoch ihren enormen Einfluss auf den Verlauf von MS im Mausmodell. Im direkten Vergleich konnte ich zudem herausstellen, dass ich die Makrophagen im Gehirn deutlich spezifischer genetisch verändern konnte, als es bisher möglich war.
Folglich können mögliche therapeutisch nutzbare Zielstrukturen speziell von Makrophagen in einer nie dagewesenen Genauigkeit überprüft werden. Dadurch wurde die Grundlage geschaffen, neue Wege zu einer erfolgreichen Behandlung von MS-Patienten zu suchen.
Peter Wieghofer wurde 1985 in Trier geboren. Von 2005 bis 2007 studierte er Biologie an der TU Kaiserslautern und von 2007 bis 2011 an der Eberhard Karls Universität Tübingen. Nach seiner Diplomarbeit am Hertie Institut für klinische Hirnforschung in Tübingen forschte er am Institut für Neuropathologie in Freiburg. Seine dort angefertige Dissertation mit dem Thema “Origin, Fate and Function of Macrophages in the Central Nervous System in Health and Disease” verteidigte er im Februar 2016 erfolgreich. Heute arbeitet er am Institut für Anatomie in Leipzig.


Sehr spannend, auch wenn ich bestimmt nicht alles verstanden habe. Wenn die Mikrogliazellen als Wächter und gleichzeitig als Architekten des Gehirns bezeichnet werden, nimmt es nicht Wunder dass deren Erkrankung (Entzündung mit einhergehender bleibender Veränderung?) zu allen möglichen Gehirnerkrankungen führen kann.
Falls man erkrankte Mikrogliazellen gentechnisch reparieren und züchten kann, um damit erkrankte Mikroglia zu ersetzen, wäre das ein vielversprechender Weg um nicht nur MS sondern auch diverse, altersbedingte Gehirnerkrankungen wie auch Demenz zu bekämpfen?
” Schon vor der Geburt beeinflussen Mikroglia die entstehenden Nervenzellen und wie sich diese miteinander verknüpfen…”
Wie ist das zu verstehen ? Besitzen diese Mikroglia einen genetischen Code um zum Beispiel unbewusste Verhaltensmuster ( Instinkte/ Reflexe /Triebe) hiermit im Nervensystem zu installieren ? Normalerweise werden Nervenzellen durch bewußte und unbewusste Lernprozesse (Hebbsche Regel) miteinander verknüpft.Letzteres würde dann aber auch bedeuten, dass bereits im embryonalen Stadium wichtige Lernprozesse stattfinden ? Theoretisch könnte dann hier bereits von einem Stadium der PRÄGUNG gesprochen werden ?