Rekombinase wechsle dich
Ich habe es gelesen! Ihr wisst schon, das Paper mit der molekularen Schere und HIV und so. Hat CRISPR doch die Welt gerettet? Weit gefehlt! Die Forscher aus Dresden und Hamburg haben die schon lange verwendeten Rekombinasen für ihre Zwecke benutzt. Rekombinasen sind Enzyme, die in Bakterien und Pilze natürlich vorkommen und dort spezifische Zielsequencen erkennen und den direktionalen Austausch von kurzen DNA-Sequencen zwischen 30-40 Basenpaaren vermitteln. Das heißt, dass diese Sequencen je nach Rekombinase z.B. “umgedreht” oder ganz ausgeschnitten werden. Rekombinasen werden auch gerne im Labor verwendet. Sagen wir, ich möchte eine Sequenz in ein Genom einbringen und um die Auswahl veränderter Zellen zu erleichtern, bringe ich zusätzlich einen Selektionsmarker ein, damit nur Zellen überleben, die auch die Veränderung tragen. Wenn mein Experiment erfolgreich war und ich Zellen gefunden habe, die die Zielsequenz in ihr Genom integriert haben, benötige ich den Selektionsmarker nicht mehr. Um ihn nachträglich wieder entfernen zu können, trägt er die Rekombinationssequenzen vor und hinter seiner Sequenz. Gibt man die passende Rekombinase dazu, schneidet diese die entsprechende Sequenz aus, bzw. invertiert und inaktiviert sie damit. Eine typischerweise verwendete Seqeunz wird als LoxP bezeichnet. Die LoxP-Sequenz stammt aus einem Virus (bzw. einer Bakteriophage). Das zur Einleitung.
Unsere Forscher waren auf der Suche nach einem Weg um den HI-Virus, der sich in das Genom von bestimmten Immunzellen integriert, wieder zu entfernen um Patienten final zu heilen. Und Rekombinasen eignen sich dazu ganz großartig. HIV gehört zu den Lentiviren, die während der Integration ins Genom deren eigene Sequenz von den sogenannten long terminal repeats (LTRs) flankieren, die den Virus dazu befähigen wieder aus dem Wirtsgenom “auszutreten” um neue Viren zusammen zu bauen. Und genau diese Sequenzen sollten genutzt werden um HIV endgültig zu entfernen. Eine Analyse dieser LTR-Sequencen in verschiedenen Patienten identifizierte eine Sequenz, die sich in 90% der HIV-Subtypen fand und die entfernt an die LoxP-Seqeunz erinnerte und von den Wissenschaftlern LoxBTR getauft wurde. Die HIV-Sequenz LoxBTR wich in 23 von 34 Basenpaaren von LoxP ab. Normalerweise schneidet die Cre-Rekombinase LoxP-Sequencen. Das ist durch die Abweichungen von der eigentlichen LoxP-Sequenz allerdings nicht möglich. Um eine Rekombinase zu erzeugen, die die entsprechende HIV-Sequenz erkennt wurde directed evolution verwendet. Diese Methode wird angewandt, wenn nicht genau klar ist, wie ein Protein verändert werden kann um einen gewünschten Effekt zu erzielen. Directed Evolution vollzieht dabei “normale” Evolution quasi im Kleinen nach. Dafür benötigt es zunächst einen Pool (eine Auswahl) von möglichen Variationen, die unterschiedliche Auswirkungen auf die “fitness” (also unterschiedliches Verhalten unter Selektionsbedingungen aufweisen) und dass die Eigenschaft vererbbar ist. Und fertig ist der Evolutionsbaukasten. Zusammenfassen lässt sich die Idee ganz einfach so: die Cre-Rekombinase erkennt LoxP, soll aber LoxBTR erkennen.
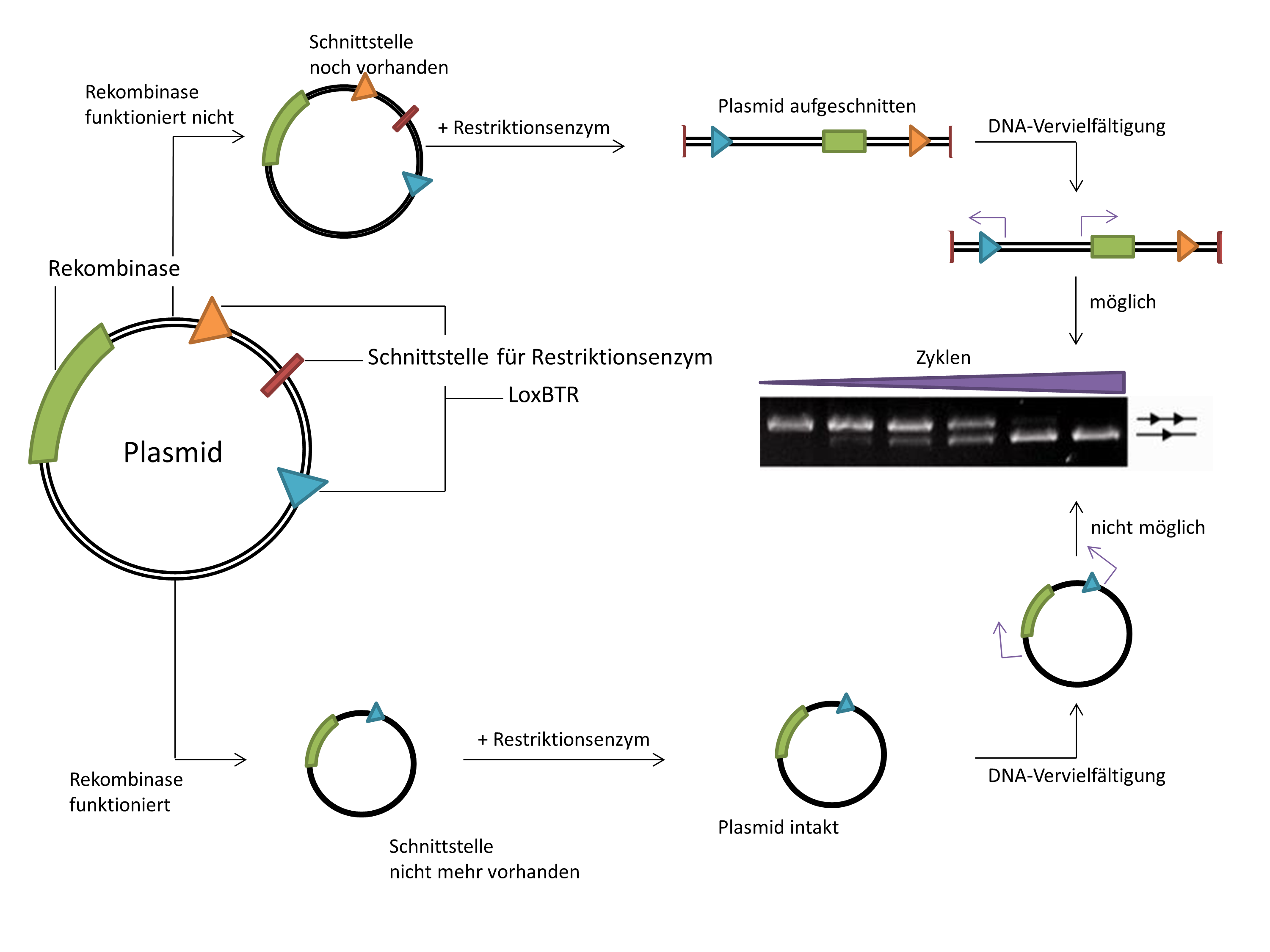
Im ersten Schritt wurde die Cre-Sequenz genommen und willkürlich mutiert. Das kann z.B. durch Bestrahlung mit UV-Licht oder durch gewollt fehlerhafte Vermehrung der gewünschten DNA-Sequenz erfolgen. Man erhält in der Folge immer noch das gleiche Gen, aber in vielen Varianten mit verschiedensten Mutationen. Das bezeichnet man als library, oder Bibliothek. Diese wurde dann in Plasmid-DNA eingebracht (Zur Erinnerung: Kreisförmige DNA, die in Bakterien vorkommt und gerne im Labor für allerlei Unfug missbraucht wird). Die Wissenschaftler verwendeten dafür nicht einfach irgendeine Plasmid, sondern ihre eigene Idee, die sie schon vor mehr als 15 Jahren das erste Mal publiziert haben. Auf diesen Plasmiden befinden sich nämlich gleichzeitig auch die LoxBTR-Sequenzen, die durch die neue Rekombinase erkannt werden sollen. Dabei trägt jedes Plasmid eine andere Rekombinase-Mutation. Man überprüft (screent) dann eine große Anzahl von möglichen Sequenzen, also mutierten Rekombinasen, bis man eine findet, die ihren Job ganz gut macht und verbessert die dann nach und nach. Eine weitere Besonderheit des für das Screening verwendete Plasmids ist, dass sich zwischen den LoxBTR-Sequenzen eine Schnittstelle für ein spezifisches Restriktionsenzym befindet (in der Abbildung unten in rot). Was soll das? Ich habe das Prinzip unten mal schematisch aufgezeichnet. Leider kann ich die Originalbilder nicht verwenden… Die Idee dahinter ist folgende: wenn die mutierte Rekombinase die LoxBTR-Seqeunz erkennt, entfernt sie den Bereich und hinterlässt nur die zweite Erkennungssequenz (in der Abbildung türkis) und die Schnittstelle für das Restriktionsenzym ist weg. Dadurch kann das kreisförmige Plasmid nicht geschnitten werden und das Plasmid bleibt intakt. Im letzten Schritt wird dann versucht die DNA von den geschnittenen bzw. noch intakten Plasmid zu vermehren (der Bereich zwischen den lila Pfeilen). Das ist nur möglich, wenn die Rekombinase funktioniert hat und so die Restriktionsschnittstelle entfernt wurde. Man erhält dann entweder ein oder zwei Produkte aus der DNA-Vervielfältigung. Dazu habe ich eine Abbildung aus einer anderen Veröffentlichung “geliehen”, die zeigt in etwa das, was ich gerade erklärt habe. Die obere Bande repräsentiert das Ausgangsplasmid, das sich je nachdem wie gut die Rekombinase funktioniert immer noch finden lässt. Wenn die Rekombinase die LoxBTR-Sequenz besser erkennt, kommt die zweite (untere = kleinere) Bande dazu, bis am Ende das Plasmid jedes Mal geschnitten wird und nur noch die untere Bande zu sehen ist. Die Rekombinase wird in mehreren Zyklen verbessert. Auf dem vermehrten DNA-Stück befindet sich nämlich die Sequenz der mutierten Rekombinase, die dann wieder in das Ausgangsplasmid eingebracht und durch eine weitere Methode wieder verändert wird, die ich mir jetzt mal spare zu erklären. Dadurch erhält man wieder einen neuen Pool an verschiedenen Rekombinasen, die dieses Mal aber schon besser die LoxBTR-Sequenz erkennen. Und dann geht das Screening nach einer passenden Rekombinase wieder von vorne los. Ich hoffe das war einigermaßen verständlich erklärt. Dieses Prozedere wiederholt man so lange, bis man die ursprüngliche Cre-Rekombinase so weit verändert hat, dass sie die LoxBTR-Sequenz mit hoher Güte erkennt und die LoxP-Sequenz nicht mehr erkannt wird. Im vorliegenden Fall wurden diese Zyklen 145-mal wiederholt. Die am Ende erhaltene Rekombinase wurde Brec-1 getauft.
Eigentlich war es das dann auch mit dem Paper. Was noch folgt sind natürlich Tests in verschiedenen Zelllinien, um sicherzustellen, dass die Rekombinase keinen negativen Einfluss auf die Zellen hat, und außerdem, dass Brec-1 auch nur LoxBTR erkennt und nicht mehr LoxP. Der erste Test, ob das Konstrukt funktioniert, wurde dann in Immunzellen, die aus HIV+ Patienten gewonnen wurden, vorgenommen. Das hat natürlich alles funktioniert, sonst wäre es ja nicht in Nature Biotech veröffentlicht worden. Am Ende wird es dann doch noch mal interessant, da geht es dann endlich ins Tiermodell.
Noch eine Bemerkung zum benötigten Zeitaufwand. Ein Zyklus für die Anpassung der neuen Rekombinase benötigt etwa 2-3 Tage. Für eine komplett neue Rekombinase müssen dann dementsprechend 1-2 Jahre Entwicklungszeit eingeplant werden. Im Vergleich zur Entwicklungszeit anderer “Medikamente” ein eher überschaubarer zeitlicher Aufwand. Praktisch ist außerdem, dass Brec-1 nicht nur so designt wurde, dass ein Großteil der zirkulierenden Subtypen von HIV erkannt werden kann, sondern dass Brec-1 sogar in der Lage ist LoxBTR mit Punktmutationen zu erkennen. Das würde zumindest am Anfang der Bildung von Resistenzen entgegen wirken. Im Vergleich zu dem derzeit so beliebten CRISPR/Cas-System und TALE Nukleasen dauert die Herstellung doch sehr viel länger, allerdings sind unspezifische Schnitte quasi auszuschließen. Problematisch könnte es für die Rekombinasen dann werden, wenn sich HIV in einzelnen Zellen mehrfach ins Genom integriert hat, was dazu führen könnte, dass die Bereiche zwischen den Viren entfernt würden anstatt die eigentlichen Virussequencen, was für die Zelle potentiell schädlich sein könnte. Doppelte Virusintegration wird allerdings nur extrem selten beobachtet. Außerdem würde alleine bedingt durch den räumlichen Abstand auf dem Genom der eigentliche Virus schon von der Logistik her sehr viel häufiger entfernt werden, als der Bereich zwischen den Viren. Und dann wäre immer noch nur ein Chromosom betroffen und das andere Chromosom wäre noch intakt. Insgesamt überwiegen die Vorteile allerdings gegenüber den denkbaren Risiken. Ich bin auf jeden Fall gespannt, ob es die Rekombinasen in eine klinische Studie schaffen werden!
Merken


Eine Folge von In-Vitro Enzymmutationen also um das “richtige” Enzym zu errraten, eine Evolution im Reagenzglas also. Trial & Error um ein Ziel zu erreichen. Ich würde eigentlich erwarten, dass man heute die gewünschte Rekombinase im Computer berechnen kann und ein Trial & Error-Verfahren nicht mehr nötig sei. Doch ich finde es schön, das so etwas klappt, dass auch der Mensch ein Ziel mit evolutionären Methoden erreichen kann – und das in 1 bis 2 Jahren.
Warum aber haben Artificial Life-Systeme/Simulationen, die sich im Computer nach evolutionären Prinzipien entwickeln bis jetzt nichts Grosses hervorgebracht? Ich denke, das liegt darin, dass die Evolution nicht besser sein kann als die Welt in der sie stattfindet. Wenn die im Computer simulierte Welt allzu primitiv ist, wird auch die Evolution in dieser primitiven Welt nichts brauchbares hervorbringen.
Was ich ausgelassen habe ist, dass die Wissenschaftler auch zeigen konnte, welche Basenpaare vorwiegend während des Evolutionsprozesses verändert wurden und dass es auch konservierte Bereiche gab. Vielleicht kann das ja zukünftig helfen eher einen ‘rational design’ Prozess zu verwenden.
Die Artificial-Life Systeme, die Sie ansprechen kenne ich leider nicht. Ohne jegliches Vorwissen klingt es für mich allerdings auch plausibel, dass der Grad der Ausgestaltung der simulierten Welt die Entwicklung dieser Systeme beeinflusst. Dazu werde ich mir auf jeden Fall mal Literatur suchen, klingt spannend!
…und wieder einmal vergessen, dass “Virus” sächlich und nicht männlich ist. Das kann man als Indikator für unzureichende Fachkompetenz werten. Was ist sonst noch falsch an dem Artikel?
Alles. Einfach alles ist falsch an diesem Artikel. Sie haben mich erwischt, ich habe mir mal wieder alles nur ausgedacht. Aber mit Ihrer umfassenden Fachkenntnis, stellt das ja für Sie kein Problem dar.
http://www.duden.de/rechtschreibung/Virus
Oh, da kann jemand mit Kritik (und wohl auch mit Lexika) nicht umgehen! In dem von Ihnen angeführten Duden-Link steht eindeutig, dass “Virus” in der Fachsprache ein Neutrum ist. Lediglich umgangssprachlich (und wohl auch, wenn Computerviren gemeint sind) verwendet man es im männlichen Geschlecht, dann kann man aber laut Duden auch “Bazille” sagen. Also möge der Verlag entscheiden, ob das hier ein Wissenschaftsblog oder eine Stammtischplauderei ist. Dann schreiben wir hier in Zukunft “die Aidsbazille” statt das HI-Virus!!
Absolut richtig! Auch die Schlussfolgerung den gesamten Inhalt in Frage zu stellen ist dem Sachverhalt angemessen. Ich möchte Sie darum bitten auch alle anderen Artikel noch einmal für mich zu lesen um eventuelle Katastrophen aufzudecken. Ich werde mich dann direkt mit meiner Alma Mater in Verbindung setzen um meine mangelhafte Sachkenntnis dort anzuprangern. Schließlich habe ich noch Studiengebühren bezahlt, da kann man wirklich besseres erwarten.
Erkennen die Rekombinasen ähnlich Sequenzabhängig wie Restriktionsenzyme. Und wenn ja, wie lang sind eigentlich die erkannten Sequenzen. Die Erkennung muss ja ein ganzes Stück komplexer sein, sonst gäbe es ja auch Probleme mit der Spezifität.
Nebenbei, der, die, das Virus ist mir auch aufgefallen, war mir aber egal, der Inhalt zählt. Liegt sicher auch daran, dass man es überall falsch hört. Und lesen wird man den Begriff auch eher in englischsprachigen Publikationen. Zumindest als Fachfrau, die den Unterschied zwischen falscher Grammatik und falschem Begriff kennt.
Restriktionsenzyme erkennen je nach Typ Sequencen zwischen 4 und 25 Basenpaaren und schneiden dann entweder direkt an der Erkennungssequenz oder im unmittelbaren Umfeld. Die im Labor verwendeten REs sind i.d.R. vom Typ II und erkennen palindromische Sequencen von meistens 6 Basenpaaren und schneiden direkt die Sequenz. Der Schnitt kann dabei ‘gerade’ sein oder überhängende Basenpaare erzeugen, was im Labor gerne wie Lego verwendet wird um damit Wunschsequencen in ein Plasmid einzubringen. Restriktionsenzyme dienen der Immunabwehr von Bakterien gegen Bakteriophagen (also Bakterien-befallende Viren).
Rekombinasen sind Enzyme, die die genetische Rekombination vermitteln. Sie sind vielfach in Pilzen und Bakterien, aber auch im Menschen zu finden, wo ihre wichtigste Aufgabe in der Reparatur von DNA-Doppelstrangbrüchen ist. Wenn wir im Labor heute von Rekombinasen sprechen, dann sind meist Cre und Flp gemeint, was etwas irreführend ist. Beide gehören nämlich zu der Integrase-Familie der orstspezifischen Rekombinasen. Die sind dann in Viren (also auch Bakteriophagen) zu finden. Zu diesen Rekombinasen gehört immer auch eine spezifische Erkennungssequenz. Natürlicherweise benötigen Viren Integrasen um sich ins Wirtsgenom zu integrieren. Die Erkennungssequenz LoxP ist 34 Basenpaare lang und im weitesten Sinne ein Palindrom. Dabei stammen Cre und LoxP eigentlich aus zwei verschiedenen Bakteriophagen. Um 1990 konnte allerdings gezeigt werden, dass Cre in der Lage ist genomische Bereiche, die von zwei LoxP-Sequencen eingeschlossen sind, “ausschneiden” können, was ein großartiges Tool für die Molekulargenetik darstellt. Je nach Design können die mittleren Seqeuencen aber auch z.B. invertiert werden, was wieder andere Anwendungsmöglichkeiten mit sich bringt.
Ich hoffe, das reicht als Erklärung.
Es stimmt übrigens dass in meinem Sprachgebrauch der/die/das Virus nicht vorkommt. Gelesen prinzipiell nur in englischer Sprache und ansonsten wird immer nur von ‘Viren’ in der Mehrzahl gesprochen. Und, danke 😉