Unterschätzte Minerale: Pyrochlor
BLOG: Mente et Malleo

Auch wenn Pyrochlor, der noch besser: die Minerale der Pyrochlor-Gruppe, zu den wichtigeren Erzen gehören, sind sie selber bislang wohl vergleichsweise unbekannt. dabei dürften die meisten von uns mehr oder weniger Nutznießer dieses Minerals sein. Besonders, wenn sie einen Computer oder ein modernes Smart-Phone oder dergleichen ihr eigen nennen.
Pyrochlore vom Karbonatitvorkommen Panda Hill im Süden Tansanias. Eigenes Foto, CC-Lizenz.
Die Pyrochlor-Gruppe beinhaltet eine Serie verschiedener kubisch kristallisierender Minerale, die zumeist größere Mengen von Niob, Tantal und Titan enthalten. Dabei sind vor allem Niob und besonders Tantal von besonderem wirtschaftlichem Interesse.
Tantal zum Beispiel ist mit seinem extrem hohen Schmelzpunkt von 2996 °C und seinem Siedepunkt von 5429 °C extrem temperaturbeständig. Hinzu kommt, dass es auch gegenüber Säuren und Basen sehr beständig ist und erst ab rund 150 °C von diesen angegriffen wird. Diese Stabilität gegenüber chemischen Einflüssen macht das Metall für Einsätze im medizinischen Bereich sehr interessant, ebenso wie in Legierungen für stark beanspruchte Bauteile.
Außerdem hat Tantal (genau genommen eine dünne, stabile, hoch permittive, isolierende Tantal(V)-oxid-Schicht (Ta2O5), danke an Karl Bednarik für die Präzisierung) eine sehr hohe elektrische Kapazität und kann daher elektrische Ladungen speichern, womit dieses Metall auch für die Elektronik interessant. In den meisten unserer technischen Produkte, vom Computer bis hin zur neuesten Smart-Phone Generation kommt kaum etwas ohne Tantal-Kondensatoren aus. Dies hat, zusammen mit der starken Verbreitung der elektronischen Geräte zwischenzeitlich dazu geführt, dass Tantal um das Jahr 2000 teurer als Silber wurde und über 500 $ pro Kilogramm kostete. Auch heute liegt der Preis noch deutlich über 300 $ pro Kilogramm. Denn Tantal ist ein sehr seltenes Element, es hat in der kontinentalen Erdkruste nur einen Anteil vom 8 ppm.
Ein Großteil des Tantals wird aus dem mittlerweile berühmt-berüchtigten Erz “Coltan” gewonnen, welches durch die Konflikte in der heutigen Demokratischen Republik Kongo bekannt wurde. Das Wort ist ein “Hybrid” aus den Namen der Endglieder der zugehörigen Erzminerale Columbit und Tantalit. Diese sind, zumindest teilweise, ein Verwitterungsprodukt unserer Pyrochlore (das wird Thema eines eigenen Blogposts werden).
Bleiben wir also vorläufig bei der Mineralfamilie der Pyrochlor-Gruppe. Das Mineral Pyrochlor selbst wurde 1826 von WÖHLER (1826) erstmals beschrieben. Sein Name setzt sich aus dem griechischen pyr = Feuer und chloros = grün zusammen, da sich das Mineral beim Erhitzen meist gelbgrün verfärbt. Die in der Gruppe zusammengefassten Minerale zeigen eine große Variabilität hinsichtlich ihrer chemischen Zusammensetzung, die von dem jeweiligen Druck, der Temperatur und den flüchtigen Komponenten zum Zeitpunkt der Bildung abhängig ist. In den natürlichen Vorkommen werden sie durch die Pyrochlor-, Betafit- und Mikrolith-Untergruppen vertreten und stellen die mit am weitesten verbreiteten Minerale der Seltenen Erden dar.
Wie variabel ihre Zusammensetzung ist, zeigt sich in der generellen Formel der Pyrochlore:
A2-mB2X6-wY1-n*pH2O
Dabei stehen die Buchstaben A, B und Y für verschiedene Positionen, die tiefgestellte Zahl gibt die Anzahl der Ionen an, die auf den jeweiligen Stellen Platz finden. Auf den ersten Blick verwundern sicher die neben den Zahlen stehenden m und n, die subtrahiert zu werden scheinen. Die Pyrochlore können durchaus damit leben, dass nicht alle möglichen Plätze in den Formeleinheiten auch belegt sind. Im Kristall werden deutliche Fehlstellen auf den A, X und Y Stellen toleriert (m = 0 – 1,7, w = 0,7, n = 0 – 1), wobei Wanderungen der Ionen innerhalb der Gitterstruktur stattfinden können. Defekte Pyrochlore können durch die Aufnahme von Wassermolekülen (p = 0 – 2) und OH-Gruppen stabilisiert werden.
Dieses Verhalten macht die Minerale relativ widerstandsfähig gegenüber Umwelteinflüssen wie beispielsweise Verwitterung. Die unterschiedlichen Positionen können von den folgenden Elementen besetzt werden:
A: Ca2+, Na+, Fe2+, Ba2+, Seltene Erden, Pb2+, Bi3+, Y3+ Th4+, U4+, K+, Mn2+, Sn2+, Sr2+, Sb3+, , und Cs+
B: Nb5+, Ta5+, Ti4+, Sn4+, Al3+, Fe3+, Zr4+, und W4+.
X: O2–, OH–
Y: O2–, OH– und F–
Das würde irgendwie zu einem reichlich unübersichtlichen Wildwuchs an möglichen Mineralnamen führen. daher haben sich findige Köpfe ein System ausgedacht, wie man da trotzdem ein wenig Ordnung hinein bekommt. Zum Beispiel, indem man sich auf die drei ersten B-Positions-Ionen beschränkt (fett markiert), also die Elemente Tantal, Niob und Titan.
So wird die Pyrochlor-Gruppe bezüglich des Gehaltes an den Elementen Niob, Tantal und Titan in drei Untergruppen unterteilt:
Mikrolith mit 2Ti < Nb + Ta und Ta ≥ Nb
Betafit mit 2 Ti >> Nb + Ta und Ta ≥ Nb
Pyrochlor mit 2 Ti < Nb + Ta und Nb > Ta
Das Bedeutet eigentlich nichts anderes, als dass Pyrochlor (das Mineral, nicht die Gruppe) Niob-dominiert ist, während die Tantal-haltigen Mitglieder der Familie als Mikrolithe, die Titan-haltigen als Betafite bezeichnet werden.
Doch damit hat sich das Benennen noch lange nicht. Wie oben bereits angesprochen, sind die Mitglieder der Familie in ihrer Zusammensetzung recht variabel. Und um die Unterscheidungen noch etwas mehr auf die Spitze zu treiben, kann man die jeweiligen Untergruppen noch nach der Belegung der A-Position einteilen.
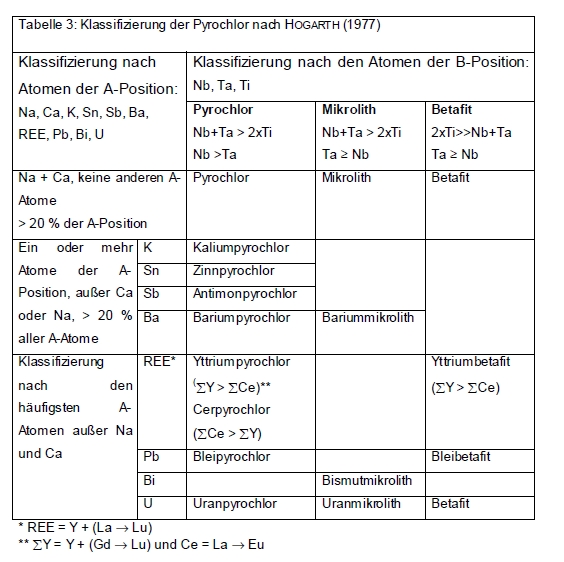
Mögliche Namen für Mitglieder der Pyrochlor-Mineralfamilie nach Hogarth 1977.
Die Mitglieder der Pyrochlor-Untergruppe kommen hauptsächlich in Karbonatiten, Nephelinsyeniten und granitischen Pegmatiten vor. Durch diese unterschiedlichen Wirtsgesteine zeigen die Mitglieder der Pyrochlor-Untergruppe eine relativ hohe Variabilität in ihrer chemischen Zusammensetzung. Sogar innerhalb eines Vorkommens kann die Zusammensetzung der Pyrochlore deutlichen Schwankungen unterliegen.
Natürliche Pyrochlore zeigen üblicherweise eine sehr schlechte Spaltbarkeit, meist nach den Oktaederflächen, die sich besonders in Dünnschliffen offenbart. Der Bruch ist muschelig, wellig, oft auch zersplittert. Makroskopisch zeigen sie einen Glasglanz auf den Prismenflächen, auf den muscheligen Bruchflächen auch Fettglanz. Die Mohs´sche Härte beträgt 5 bis 5,1, kann aber auch deutlich niedrigere Werte annehmen, wenn das Mineral metamiktisiert oder verwittert ist.
Die Dichte von Mitgliedern der Pyrochlor-Familie beträgt von 4,2 bis 6,3 g/cm3, wobei die Dichte mit dem Gehalt an Tantal proportional zunimmt.
Bestimmte Unterspezies können deutlich höhere Werte für die Dichte erreichen. So sind Blei-Mikrolithe beschrieben worden, deren Dichte 7,2 beträgt.
“Nelkenbrauner” Pyrochlor vom Karbonatit von Sukulu, Uganda. Eigenes Foto, CC-Lizenz.
Unter dem Polarisationsmikroskop zeigen sich die Minerale der Pyrochlor-Gruppe aufgrund ihres kubischen Kristallsystems isotrop. Es kann aber zuweilen eine anomale schwache Doppelbrechung bei nicht metamiktisierten Mineralen beobachtet werden. Schon bei nur oberflächlicher Durchmusterung von Dünnschliffen fallen die Pyrochlore dank ihrer charakteristischen nelkenbraunen Farbe (mit linearen Polarisatoren), ihrer meist idiomorph-oktaedrischen Ausbildung und ihrem isotropen optischen Charakter sowie der relativ hohen Lichtbrechung (n = 1,96 – 2,18) schnell ins Auge.
Die Minerale der Pyrochlor-Gruppe sind nicht nur aufgrund ihrer Gehalte an Niob (Sonderstähle und Nukleartechnik) und Tantal (Kondensatoren, Mikroelektronik) von besonderem Interesse. Und sie sind ein hervorragendes Beispiel dafür, dass man mit Mineralogie, also dem Wissen über Minerale eine ganze Menge anfangen kann.
Phasen mit Pyrochlorstruktur (A2B2X6Y1-Strukturen) zeigen eine breite Palette interessanter physikalischer Eigenschaften und lassen sich zudem vergleichsweise einfach synthetisieren. Dabei können Übergangsmetalle unterschiedlicher Oxidationsstufen sowie die auf die im Periodensystem den Übergangsmetallen folgenden Metalle B-Positionen besetzen und die A-Positionen werden sowohl von Elementen der Seltenen Erden oder Elementen mit inertem „freien Elektronenpaar“ eingenommen. Die elektrischen Eigenschaften dieser Pyrochlore (die verschiedenen in der Pyrochlorstruktur kristallisierenden Phasen der Einfachheit werden der Einfachheit halber alle als Pyrochlor bezeichnet, unabhängig von der mineralogischen Terminologie) reichen von isolierend über halbleitend bis hin zu leitend und den jeweiligen Übergängen. Ebenso sind Pyrochlore mit verschiedenen magnetischen Eigenschaften bekannt oder mit guter Hitzebeständigkeit. Defektstrukturen zeigen eine gute kationische Leitfähigkeit und stellen Festkörperelektrolyte dar. Phasen mit Defektstruktur, die 4d oder 5d-Übergangsmetallen auf der B-Position haben, werden aufgrund ihrer ausgezeichneten ionischen (O2-) und elektronischen Leitfähigkeit als Sauerstoffelektroden bezeichnet und bieten unter anderem neue Ausblicke im Bereich der Brennstoffzellen.
Ln-haltige Pyrochlore zeigen Fluoreszenz und Phosphoreszenz und finden eine mögliche Verwendung in der Lasertechnik. Aufgrund ihrer relativ hohen Beständigkeit gegenüber Verwitterungsprozessen wurden sie verschiedentlich für eine Immobilisierung von nuklearen Abfällen vorgeschlagen
Hogarth, D. D., 1977. Classification and nomenclature of the pyrochlore group. American Mineralogist 62, 403 – 410.



Tantal(V)-oxid
Nicht das Tantal selbst hat eine sehr hohe elektrische Kapazität, sondern eine dünne, stabile, hoch permittive, isolierende Tantal(V)-oxid-Schicht (Ta2O5).
Streng genommen gilt der Begriff der Kapazität nur für den gesamten Tantal-Elektrolytkondensator.
[ so tief war ich in die elektrischen Eigenschaften von tantal und Tantaloxiden garnicht eingestiegen. Das wäre sicher ein ganzes Thema für sich. Danke (GR)]
Wo ist das X in der Formel?
Wenn die generelle Formel, wie im Text angegeben,
A2-mB2Y1-n*pH2O
lautet, woher kommt dann das weiter unten genannte X? (X: O2-, OH-)
Bitte um Aufklärung!
Danke!
[Hoppla, da hat es das X irgendwie beim übertragen zerlegt. Formel korrrigiert, Danke für den Hinweis (GR)]
spin ice
Danke fuer diesen interessanten Artikel.
Auch ziemlich bemerkenswert ist, dass die besondere Struktur des Pyrochlor-Gitters frustrierte magnetische Systeme erlaubt, in denen magnetische Monopole auftreten koennen.
Pyrochlor
Bin dabei, mich auf einen Vortrag über den Unterschied von Karbonatiten und Urkalken vorzubereiten, da hilft mir dein Artikel auch weiter.Danke.
Renate Bönig-Müller von der AG für Geologie und Geschiebekunde in Lüneburg
Bin dabei, mich für einen Vortrag über Urkalk und Karbonatit vorzubereiten für die Kristallin-Gruppe. Dein Beitrag hat mir weitergeholfen.
Pyrochlor
Warum ist ein Vorkommen von Pyrochlor im Urkalk nicht möglich?
@ Renate
Dazu fehlen in den Urkalken schlicht die notwendigen Elemente wie Niob und Tantal. Tantal ist ein extrem seltenes Element, es rangiert im Vorkommen in der Erdkruste von rund 80 stabilen Elementen in der Erdkruste auf Platz 50.