Diabetes: Stress kann Betazellen reversibel verändern
BLOG: Medicine & More

Vielleicht sind die meisten Insulin-produzierenden Betazellen bei Vorliegen eines Typ-2-Diabetes gar nicht unwiederbringlich zerstört, sondern lediglich reversibel zurückgebildet? Ein Forscherteam hat am Mausmodell eine erste Bestätigung für diese interessante Hypothese gefunden. Die Erkenntnisse könnten in Zukunft die Diabetes-Therapie deutlich verbessern.
Zivilisationskrankheit Diabetes mellitus
Diabetes mellitus (von altgriechisch διαβαίνειν “hindurchfließen” und lateinisch mellitus “honigsüß”, umgangssprachlich Zuckerkrankheit), ist eine chronische Stoffwechselerkrankung, an der weltweit etwa 285 Millionen Menschen leiden. In Europa gibt es rund 55 Millionen Diabetiker, Tendenz steigend. In Europa steht Deutschland mit 12 Prozent Zuckerkranker unter den 20 bis 79-Jährigen an der Spitze.
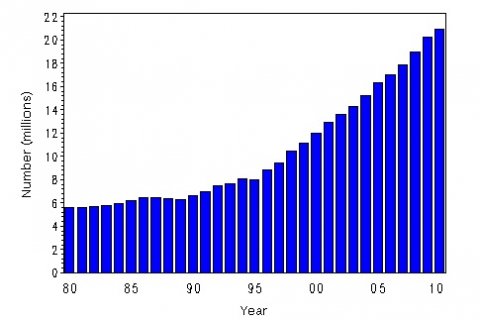
Wohlstandskrankheit: Anstieg der Diabetiker von 5.6 auf 20.9 Millionen in den USA, 1980-2010 (Daten: Centers for Disease Control and Prevention).
Die beiden wichtigsten Formen sind der Typ-1- und der Typ-2-Diabetes. Leitbefund ist die Überzuckerung des Blutes (Hyperglykämie), erste Symptome sind oft starker Harndrang und ständiger Durst.
Diabetes Typ 1
Der Typ-1-Diabetes beginnt meist schon im Kindes- und Jugendalter. Es besteht ein absoluter Mangel am Insulin, dem Hauptregulierungshormon des Zuckerstoffwechsels. Ursache ist in der Regel eine Fehlreaktion des Immunsystems, die zu einer Zerstörung Insulin-produzierender Betazellen der Langerhans-Inseln in der Bauchspeicheldrüse und damit zu einem absoluten Insulinmangel führt. Dadurch steigt der Blutzuckerspiegel und die Patienten müssen Insulin spritzen.
Diabetes Typ 2
Etwa 95 Prozent der Diabetiker leiden allerdings an Typ-2-Diabetes. Übergewicht, ungesunde Ernährung und mangelnde Bewegung, sowie die gesteigerte Lebenserwartung gelten als Risikofaktoren, im Laufe des Lebens einen Typ-2-Diabetes zu entwickeln. Kennzeichen ist ein relativer Insulinmangel durch eine abgeschwächte Wirkung des Insulins (Insulinresistenz).
Neben weiteren Faktoren wie Nikotinabusus, genetischer Veranlagung oder der Therapie mit bestimmten Medikamenten (z.B. Glucocorticoide oder Chemotherapeutika), erhöht auch der in der Schwangerschaft auftretende Gestationsdiabetes das Risiko, später an einem Typ-2-Diabetes zu erkranken. Hier spielen neben einer entsprechenden Genetik schwangerschaftsbedingte Hormonveränderungen, Stoffwechselbelastungen und die häufig nach Ende der Schwangerschaft bleibende Gewichtszunahme eine Rolle.
Beim Typ-2-Diabetes ist die Umstellung der Lebensgewohnheiten maßgeblicher Teil der Therapie. Dazu zählen der Abbau von Übergewicht durch körperliche Bewegung und eine ausgewogene Ernährung. Reichen diese Maßnahmen nicht aus, um den Blutzuckerspiegel zu normalisieren, können zusätzliche Medikamente, die sogenannten oralen Antidiabetika, helfen. Ist jedoch die Insulinproduktion der Bauchspeicheldrüse schließlich erschöpft, wird oft auch hier eine Insulintherapie erforderlich.
Verlauf und Prognose hängen bei allen Formen im Wesentlichen davon ab, wie gut der Blutzuckerspiegel im Normbereich gehalten werden kann. Gelingt dies und erfolgt die Diagnose rechtzeitig, ist die Prognose gut. Risiken bestehen jedoch vor allem in den Folgeerkrankungen durch eine zunehmende Schädigung der Gefäße. Oft sind beispielsweise die Füße (diabetischer Fuß) oder Augen (diabetische Retinopathie) von einer Gefäßveränderung betroffen. Häufige Todesursachen von Diabetikern sind Herzinfarkt, Schlaganfall und Nierenversagen.

Stress pur für die Bauchspeicheldrüse: Zucker und Fett nach Wurst und Wein.
Diabetes-Mäuse: Gestresste Betazellen ruhen sich aus
Angesichts der erheblichen medizinischen, sozialen und ökonomischen Auswirkungen des Typ-2-Diabetes werden dringend Verbesserungen in Vorbeugung, Früherkennung und Therapie benötigt. Darum ging es auch auf der 48. Jahrestagung der European Association for the Study of Diabetes (EASD), die letzte Woche in Berlin stattfand.
Eines der Highlights, die dort vorgestellt wurden, waren die Ergebnisse einer Studie von Dr. Chutima Talchai vom Columbia University Medical Center (CUMC) in New York. Anhand eines Mausmodells konnte die Arbeitsgruppe zeigen, dass die meisten Betazellen bei der Manifestation eines Typ-2 Diabetes wie bisher vermutet gar nicht tot sind, sondern nur kein Insulin mehr produzieren, weil sich ihre Differenzierung verändert hat.
FOXO1
Eine Schlüsselfunktion hat dabei das Transkriptionsfaktorprotein FOXO1 (Forkhead-Box-Protein O1), da es den Zuckerstoffwechsel an mehreren Stellen reguliert.
Wird nun der Stoffwechsel wiederholt oder chronisch gestresst, beispielsweise durch Schwangerschaften, Übergewicht, während des normalen Alterungsprozesses und auch in frühen Diabetesstadien, wandert FOXO1 aus dem Zytoplasma in den Zellkern. Dies konnten Dr. Talchai und ihre Kollegen in einem Mausmodell, in dem FOXO1 nicht exprimiert wird, mithilfe von Zelltracing nachweisen.
In der Folge wird FOXO1 im Zellkern vermehrt, was zu einer verstärkten Insulinsekretion der Zelle führt. Hält der Stress an, entgleist das System. FOXO1 ist dann nicht mehr nachweisbar. Die Betazelle verwandelt sich in eine Art Vorläuferzelle, die kein Insulin mehr produziert. Ein Teil der Zellen beginnt sogar Glucagon auszuschütten, einen Gegenspieler des Insulins. Dies entspricht der Stoffwechselsituation eines Typ-2-Diabetikers.
Tod auf Raten?
Die Ergebnisse lassen vermuten, dass Typ-2-Diabetes nicht durch die Zerstörung der Betazellen entsteht, sondern durch ihre Rückbildung infolge des Fehlens von FOXO1. Stimmt diese Vermutung, müsste es auch möglich sein, die Zellen wieder in ihren ursprünglichen Zustand zurückzuversetzen. Für diese Hypothese spricht auch die Beobachtung des so genannten “Honeymoons”, der “Flitterwochen” in der frühen Phase der Insulintherapie des Typ-1-Diabetes, in der sich die Betazellen durchaus wieder erholen können.
Für die Erkenntnis, das reife Zellen in ein unreifes Stadium zurückprogrammiert werden können, erhielten die Forscher Shinya Yamanaka und John Gurdon vor kurzem den Medizin-Nobelpreis. Auch die Betazellen scheinen sich ähnlich wie Stammzellen zu Vorläuferzellen zurückzubilden. Ihr Vorkommen in erwachsenen Mäusen war eine Überraschung.
Mark A. Atkinson vom Diabeteszentrums der University of California, San Francisco, hat ebenfalls Hinweise, dass Stress die Insulin-produzierenden Zellen dazu veranlassen kann, in einen unreiferen Status zurückzufallen. Chronische Überforderungen des Stoffwechsels können dazu führen, dass die Betazellen zunächst quasi eine Verschnaufpause in einem weniger aktiven Zustand einlegen wollen.
Diese Vorläuferzellen können sich dann später wieder zu anderen aktiven Zellen entwickeln, darunter auch Betazellen. Studien am Mausmodell konnten beispielsweise zeigen, dass ein Verlust einer großen Anzahl von Betazellen dazu führt, dass auch Glucagon-produzierende Alphazellen in Betazellen umgewandelt werden können. Eine andere Studie ergab, dass die Behandlung normalerweise nicht Hormon-produzierender Drüsengangzellen der Bauchspeicheldrüse mit einem Transkriptionsfaktor zur Folge hatte, dass diese Zellen in Betazellen umgewandelt wurden.
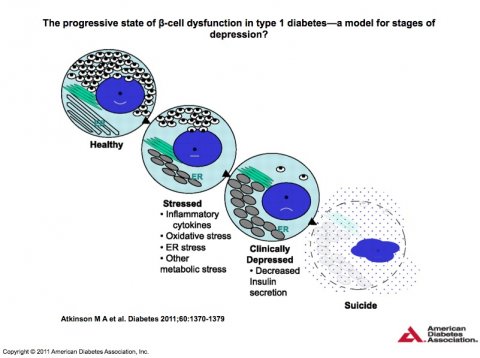
Modell für die stressinduzierte progressive Fehlfunktion der Betazellen, die zunächst zur verminderten Insulinproduktion und schließlich zum Absterben der Zellen führt. (© 2011 American Diabetes Association, Inc.)
Hoffnung für die Zukunft
Die Ergebnisse zeigen, dass die Bauchspeicheldrüse kein statisches Organ ist, sondern sich viel dynamischer verhält als bisher angenommen. Diese zelluläre Plastizität könnte zukünftig für therapeutische Ansätze genutzt werden, indem beispielsweise Vorläuferzellen in funktionale Betazellen umgewandelt werden.
Neben der vielversprechenden Stammzelltherapie haben meine Blognachbarn Sebastian Reusch (Enkapsis) und Lars Fischer (Fischblog) gerade hier und hier einen weiteren interessanten Ansatz beschrieben: Den Einsatz eines neu erzeugten Enzyms namens “Transcription Activator-Like Effector Nuclease” kurz TALEN, das falsch funktionierende Zellen wieder funktionstüchtig machen kann. Das Prinzip klingt einfach: Die Gene, welche die Zelle zu einer falschen Aktivität verleiten, werden ausgeschnitten und durch solche ersetzt, die sie wieder richtig funktionieren lassen.
Im Moment ist das Problem, auf welche Weise diese Vorläuferzellen effizient in funktionstüchtige Betazellen umgewandelt werden können, noch eine echte Herausforderung. Seine Lösung lässt jedoch schon heute auf eine bessere Diabetestherapie hoffen. Dennoch bleibt trotz allen Fortschritts in der Behandlung die Vorbeugung durch einen gesunden Lebenswandel mit viel Bewegung auch in Zukunft das beste Mittel gegen Diabetes Typ 2.
Quelle / weiterführende Literatur:
- Atkinson MA, et al.: How Does Type 1 Diabetes Develop? The Notion of Homicide or β-Cell Suicide Revisited. Diabetes May 2011 vol. 60 no. 5 1370-1379. doi: 10.2337/db10-1797
- Polonsky KS: The Past 200 Years in Diabetes. N Engl J Med 2012;367:1332-40. doi: 10.1056/NEJMra1110560
- Talchai C, et al.: Pancreatic β Cell Dedifferentiation as a Mechanism of Diabetic β Cell Failure. Cell. 2012 Sep 14;150(6):1223-34. doi: 10.1016/j.cell.2012.07.029.
- Thorel F, et al.: Conversion of adult pancreatic α-cells to β-cells after extreme β-cell loss. Nature 464, 1149-1154 (22 April 2010) | doi:10.1038/nature08894.
- Zhou Q, et al.: In vivo reprogramming of adult pancreatic exocrine cells to β-cells. Nature 455, 627-632 (2 October 2008) | doi:10.1038/nature07314.
- EASD-Kongress-Dossier


Diabetes
Dieser Artikel ist sehr gut zusammen gefasst und informativ geschrieben. Was ganz wichtig ist ist, dass man Diabetes rechtzeitig erkennt und dagegen etwas unternimmt.
Nach der Schwangerschaft meines ersten Kindes bekam ich Diabetis Typ-2, nehme seither Blutzuckersenkende Tabletten und messe regelmäßig meinen Blutzucker. Man kann gut damit leben, aber kleine Anfälle, die mich manchmal umhauen, gibt es immer.
Hatte vor 3 Jahren auch die Diagnose bekommen, was natürlich erstmal ein Schock war. Aber man lernt mit der Krankheit umzugehen. Auch ich muss regelmäßig meinen Blutzucker messen und nehme Tabletten.
Pingback:Deutschland: Vorsicht, Fußballfieber! » Medicine & More » SciLogs - Wissenschaftsblogs
Was bei Berichten über und zu Diabetes 2 seltenst angesprochen wird, ist die Rolle, die ein Mangel an Vitamin D3 – eigentlich ein Hormon – auch dabei spielt.
Dazu gibt es Literatur von Dr. Raimund van Helden und Dr. Nicolai Worm.
Sehr informativer Beitrag! Vielen Dank fürs teilen!
Ein kleines Gedicht über die Zuckerkrankheit:
DIABETES MELLITUS
Ganz und gar nicht süß
Ist die Zuckerkrankheit.
Nein,sie ist einfach fies,
Doch niemand ist gefeit.
Sich etwas mehr bewegen,
Wirkt dem Unheil entgegen.
Beim Essen mal maßhalten,
Kann Widerstand entfalten.
Die Zellen brauchen Insulin,
Sonst ist die Freude rasch dahin.
Nicht süß darf werden das Blut,
Das tut keinem von uns gut.
Unser Kreislauf kommt in Not,
Der Zusammenbruch droht.
Zu beherrschen die Lage,
Spritzt man sich alle Tage.
Schon Kinder sind betroffen;
Millionen Menschen hoffen,
Dass nun bald die Wissenschaft
Erfolge bei der Heilung schafft.
Rainer Kirmse , Altenburg