Fördern minimale Antibiotika-Rückstände in der Umwelt Resistenzen?
BLOG: Fischblog

Es ist unvermeidlich, dass man bei einer Antibiotika-Therapie einen Teil der eingenommenen Substanz unverändert wieder ausscheidet. Man geht eigentlich davon aus, dass diese Stoffe im Abwasser zu stark verdünnt werden, um in der Umwelt resistente Bakterienpopulationen heranzuzüchten. So ganz sicher können wir uns dessen aber nicht sein, im Gegenteil. In den letzten Jahren verdichteten sich die Hinweise, dass schon sehr geringe Mengen dieser Stoffe einen Effekt auf die Mikrobenflora verschiedener Ökosysteme haben.
![]() In Deutschland ist das Problem seit Anfang der 90er Jahre bekannt, als man erstmals Antibiotikarückstände in Oberflächengewässern fand. Die wichtigste Quelle für diese Verunreinigungen sind kommunale Abwässer, die zwischen einigen Dutzend Nanogramm und einigen Mikrogramm Antibiotika pro Liter enthalten können. Die Werte schwanken sehr stark, einerseits wegen der eingesetzten Mengen, andererseits aber auch wegen der chemischen Eigenschaften der verschiedenen Verbindungen: Während die klassischen Beta-Lactame chemisch zu instabil sind, um lange im Wasserkreislauf zu überleben, fanden Hirsch et al. 1999 sechs Mikrogramm Erythromycin in deutschem Abwasser.
In Deutschland ist das Problem seit Anfang der 90er Jahre bekannt, als man erstmals Antibiotikarückstände in Oberflächengewässern fand. Die wichtigste Quelle für diese Verunreinigungen sind kommunale Abwässer, die zwischen einigen Dutzend Nanogramm und einigen Mikrogramm Antibiotika pro Liter enthalten können. Die Werte schwanken sehr stark, einerseits wegen der eingesetzten Mengen, andererseits aber auch wegen der chemischen Eigenschaften der verschiedenen Verbindungen: Während die klassischen Beta-Lactame chemisch zu instabil sind, um lange im Wasserkreislauf zu überleben, fanden Hirsch et al. 1999 sechs Mikrogramm Erythromycin in deutschem Abwasser.
Diese Werte liegen größenordnungsmäßig etwa das Hundert- bis Hunderttausendfache unter den experimentell bestimmten Minimalen Hemmkonzentrationen, bei denen die Antibiotika das Wachstum von Bakterien in Kultur sichtbar behindern. Die Konzentrationen in Oberflächengewässern sind noch mal ein ganzes Stück niedriger, viel zu gering um Bakterien zu töten.
Resistenz ist Ballast – aber wie sehr?
In natürlichen Populationen existieren immer ein paar resistente Bakterien innerhalb der gesamten Population, deswegen sind Antibiotika in der Umwelt grundsätzlich ein Problem. Allerdings ist ein Resistenzgen in fast allen Fällen erst einmal nur Ballast für den Organismus, so dass der Schutzeffekt diese Kosten aufwiegen muss. Bisherige pharmakodynamische Modelle gehen davon aus, dass Resistenzgene bei Antibiotika-Konzentrationen unterhalb der Minimalen Hemmkonzentration ihre Kosten nicht wieder einspielen und sich deswegen nicht in Populationen ausbreiten.
Das Problem dabei ist, dass die Minimale Hemmkonzentration ein extrem grobes Instrument ist, um Effekte auf Bakterien zu bestimmen. Man ermittelt diesen Wert, indem man Mikroben über Nacht bei verschiedenen Antibiotika-Konzentrationen wachsen lässt und anschließend guckt ob überhaupt etwas gewachsen ist. Die Situation in freier Wildbahn ist jedoch eine völlig andere. Bakterienpopulationen enthalten zahllose Individuen mit unterschiedlicher genetischer Ausstattung, die alle nebeneinander wachsen, sich vermehren und um Ressourcen konkurrieren.
Sobald ein Merkmal auch nur einen geringfügigen Vorteil gegenüber anderen Stämmen bietet, werden seine Träger etwas schneller wachsen, sich schneller wieder teilen und langfristig – das heißt über hunderte oder tausende Generationen – einen beträchtlichen Teil aller Individuen ausmachen. Das ist das eigentliche Problem bei den verschwindend geringen Antibiotika-Mengen in der Umwelt: Wir wissen nicht wirklich, ob sie eben nicht doch einen kleinen Effekt auf Bakterien haben, der womöglich groß genug ist, um das Gleichgewicht zwischen resistenten und nicht-resistenten Stämmen merklich zu verschieben.
Unterschätzter Selektionsdruck
Dafür wissen wir inzwischen, dass die Hypothese mit der Minimalen Hemmkonzentration schlicht nicht haltbar ist. Im März dieses Jahres haben Forscher einen einfachen Farbtest vorgestellt, der anzeigt, ob unter bestimmten Bedingungen resistente Bakterien schneller wachsen als nicht-resistente. Praktischerweise haben sie gleich den Nachweis mitgeliefert, dass das tatsächlich bei einigen Antibiotika noch bei Bruchteilen der Minimalen Hemmkonzentration der Fall ist. Bei Ciprofloxacin noch bei einem Fünfundsiebzigstel. Bis zu welchen Konzentrationen diese Effekte anhalten, wird derzeit erforscht.
Gerade haben schwedische Mikrobiologen eine Veröffentlichung in PLoS Pathogens publiziert, die das ganze mal anhand von Salmonella enterica var. typhimurium durchexerziert. Die erste, inzwischen wenig überraschende Erkenntnis ist, dass Konzentrationen deutlich unterhalb der Minimalen Hemmkonzentration das Wachstum nicht-resistenter Bakterien deutlich bremsen, bei Tetrazyklin reduziert schon ein Dreißigstel der Konzentration die exponentielle Vermehrung um 15 Prozent. Das ist eine extrem drastische Reduktion der Fitness, die im klassischen Test nicht auffällt, aber in freier Wildbahn erhebliche Konsequenzen hat.
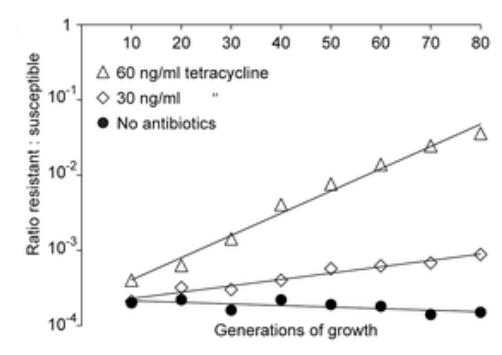
Wesentlich interessanter sind allerdings die direkten Konkurrenztests, die die Forscher durchgeführt haben. Man setzt einfach fluoreszenzmarkierte Bakterien eines resistenten und eines nicht-resistenten Stammes und eine Kulturschale und lässt sie unter Einfluss eines Antibiotikums gegeneinander wachsen. Mit einem automatischen Zählgerät haben die Forscher dann direkt ausgezählt, welcher der beiden Stämme im Verlauf der Zeit erfolgreicher war. Das kommt der realen Situation schon bedeutend näher, und auf diese Weise haben die Schweden für verschiedene Antibiotika ermittelt, ab welcher Konzentration die untersuchten Resistenzgene tatsächlich einen Selektionsvorteil bringen. Diese Konzentrationen sind durchweg niedriger als die Minimale Hemmkonzentration, in einem Fall um den Faktor 230. Ich verzichte hier darauf, die Ergebnisse im einzelnen aufzuführen, das Paper ist frei zugänglich und lesenswert.
Noch unerfreulicher ist das Ergebnis eines weiteren Versuchs, nämlich ob sich bei so niedrigen Antibiotika-Konzentrationen auch Resistenzen neu bilden und diese Stämme dauerhaft in der Population vertreten bleiben. Die Antwort ist ein ganz klares ja, und es ist nicht nur möglich, sondern unter den Bedingungen des Experiments quasi garantiert, dass Teile der Population widerstandsfähiger gegenüber dem Antibiotikum werden. Es ist auch keineswegs so, dass nur Mutanten auftauchen, die sich lediglich an die vorhandene niedrige Konzentration angepasst haben – auch der Anteil an deutlich widerstandsfähigeren Mutanten steigt im Laufe der Zeit an.
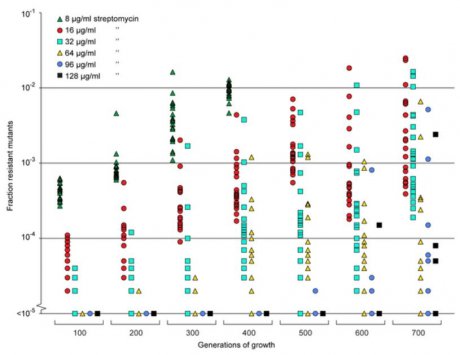
Nicht nur der Anteil resistenter Stämme nimmt mit der Zeit zu, sondern auch die Resistenz selbst. Grüne Dreiecke zeigen die empfindlichsten, schwarze Quadrate die resistentesten Stämme. Quelle: Gullberg E, et al. PLoS Pathogens 10.1371/journal.ppat.1002158, 2011
In allen Experimenten gibt es allerdings auch eine Grenzkonzentration, unterhalb derer die nicht-resistenten Bakterien einen Selektionsvorteil haben, und diese Konzentration ist in fast allen Versuchen deutlich höher als solche, die man in der Umwelt findet. Insofern sollte man mit Schlussfolgerungen im Hinblick auf Resistenzen in natürlichen Umgebungen erst einmal vorsichtig sein. Es gibt allerdings Daten, die darauf hindeuten, dass diese Effekte sehr wohl auch in freier Wildbahn auftreten, zum Beispiel resistente Bakterien in Wildtieren, die dort eigentlich nicht auftauchen sollten.
Außerdem beziehen sich die Versuche auf resistente Stämme, die sich vom Wildtyp allein durch dieses eine Resistenzgen unterscheiden. Es ist aber bekannt, dass resistente Bakterien gelegentlich zusätzliche Erbanlagen aufweisen, die den Fitnessnachteil des Resistenzgens reduzieren oder ausgleichen. Es spricht nichts dagegen, dass solche Stämme sich schon bei deutlich geringeren Antibiotika-Konzentrationen anreichern.
Diese Ergebnisse sind ein (weiterer) Warnschuss, was resistente Bakterien und ihre medizinische Bedeutung angeht. Sie bedeuten, dass Resistenzen anders als vermutet eben nicht so schnell wieder aus natürlichen Populationen verschwinden werden, wenn sie einmal entstanden sind – heutzutage sind multiresistente Erreger hauptsächlich ein Problem in Krankenhäusern, aber das wird auf Dauer anders werden, mit allen Komplikationen, die das mit sich bringt. Schlimmstenfalls muss man irgendwann routinemäßig bei jeder Infektion erstmal testen, welche Substanzen überhaupt noch wirken.
.
Gullberg, E., Cao, S., Berg, O., Ilbäck, C., Sandegren, L., Hughes, D., & Andersson, D. (2011). Selection of Resistant Bacteria at Very Low Antibiotic Concentrations PLoS Pathogens, 7 (7) DOI: 10.1371/journal.ppat.1002158


Toller Artikel
Stimt es, dass in der Tierhaltung Antibiotika präventiv eingesetzt werden, und wenn ja, ein wie großer Anteil der Gesamtproduktion? Das fände ich in dem Zusammenhang noch interessant.
Antibiotika in der Tierhaltung
Dazu kann Sören Schewe auf jeden Fall mehr sagen. Er ist immer ganz begeistert wenn das Thema aufkommt. *g*
Für den Eintrag in die Umwelt scheit die Landwirtschaft allerdings kaum Bedeutung zu haben, siehe Hirsch et al.:
Danke
genau das hat mich interessiert. Überrascht mich, ehrlich gesagt!
Hallo Maria,
mit den Antibiotika ist es wie mit dem Kraftfutter – so wenig wie möglich sollte eingesetzt werden. Bei hohen Bestandsdichten – Geflügel wird ja gerne recht dicht gehalten – kann es natürlich sein, dass ein krankes Tier entdeckt wird und dann der ganze Bestand Antibiotika bekommt, weil man schließlich nicht weiß, wo das Tier im Stall überall war und an wen es “seine” Erreger weitergegeben hat.
Eine präventive Gabe halte ich für sehr problematisch und auc ziemlich sinnlos, was ja auch Lars in seinem Artikel geschrieben hat. Und als Leistungsförderer sind sie ja mittlerwele EU-weit verboten und auch in den USA setzt langsam ein Umdenken ein.
Antibakterielle Seife in den USA
Als Ergänzung zu diesem interessanten Artikel noch einige Anmerkungen zu Antibiotika in den Oberflächengewässern der USA.
Die gute Nachricht: Es gibt zumindest in den Gewässern der USA Bakterien, die die dort am häufigsten im Haushalt eingesetzten Antibiotika Triclosan und Triclocarban, abbauen können.
(Hoffen wir, das diese Bakterien nicht schädlich für den Menschen sind.)
Die schlechten Nachrichten: Triclosan und Triclocarban reichern sich in den Nahrungsketten des Bodens und der aquatischen Ökosysteme an. Und zwar findet man umsomehr je weiter man in der Nahrungskette nach oben geht. Damit steigt natürlich der Selektionsdruck und der Anteil an stark resistenten Bakterien nimmt nach oben hin zu. In Flusskrebsen, Erdwürmern sogar Delfinen wurden diese Substanzen nachgewiesen.
Was die Bakterien locker wegstecken, scheint manchen Tieren übel auf den Magen zu schlagen. Die in den Gewässern vorliegende Antibiotikakonzentration scheint für manche Flusskrebse schon eine giftige Dosis zu sein.
Empfehlung: Auf antibakterielle Seife mit Triclosan und Triclocarban verzichten und sich mit normaler Seife waschen.
Wer sich für das Thema interessiert, hier zwei Paper aus den USA:
Evelyn Walters, Kristin McClellan, Rolf U. Halden. Occurrence and loss over three years of 72 pharmaceuticals and personal care products from biosolids–soil mixtures in outdoor mesocosms. Water Research, 2010
Todd R. Miller, David R. Colquhoun, Rolf U. Halden. Identification of wastewater bacteria involved in the degradation of triclocarban and its non-chlorinated congener. Journal of Hazardous Materials, 2010; 183 (1-3): 766