Stammzelltherapien bei neurologischen Erkrankungen
BLOG: Enkapsis

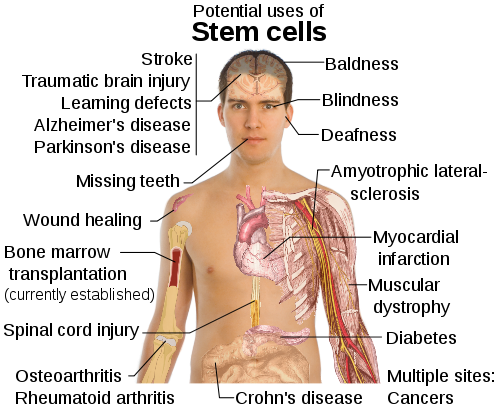
Drei bekannte Erkrankungen des Nervensystem, welches natürlich das Gehirn miteinschließt, sind Alzheimer, Parkinson und Chorea Huntington. Alzheimer ist die häufigste neurodegenerative Erkrankung bei Menschen und äußert sich molekularbiologisch dadurch, dass bestimmte Genmutationen amyloide Ablagerungen und neurofibrilläre Knäuel im Gehirn entstehen lassen, die so zu Defiziten im Kurzzeitgedächtnis und schließlich zur Demenz führen, da Neuronen zerstört werden. Parkinson zeichnet sich als zweithäufgiste neurodegenerative Erkrankung dadurch aus, dass durch eine Degeneration von dopaminverarmten Neuronen, die wiederum auf Mutationen in bestimmten Genen zurückzuführen ist, sich eine Kombination aus Zittern, Gesichtsstarre und eine Verlangsamung der Bewegungen einstellt. Neben einer weiteren Ursachendiskussion hinsichtlich bestimmten Umweltfaktoren, wie z.B. Pestiziden (aber auch anderen Substanzen in gewissen Konzentrationen), äußert sich diese Krankheit in unterschiedlichen Verlaufsformen. Chorea Huntington gehört zu einer Kategorie Krankheit, der als Auslöser sogenannte Triplettwiederholungen zugrunde liegt. Darunter versteht man, dass bestimmte Genabschnitte häufiger als normal vorkommen und so dazu führen, dass Neurone in den Basalganglien des Gehirns degenerieren, was zu motorischen Defekten führt. Damit verbunden werden Gedächtnisstörungen, Abnahme der kognitiven Fähigkeiten, Gefühlsstörungen und Persönlichkeitsveränderungen. Während sich das Krankheitsbild der Chorea Huntington meistens ab dem 40. Lebensjahr offenbart, sind die ersten Symptome bei Alzheimer und Parkinson erst ab dem 65. Lebensjahr zu erwarten. Da mit einer sich ständig nach oben verschiebenden Lebenserwartung diese Krankheiten wohl immer öfter äußern werden, sollte man der Natur nicht ihren Lauf lassen, wie es doch manchmal gesagt wird und man sollte sich um klinische Studien bemühen mit denen man diese Krankheiten versucht zu behandeln. Besonders für Betroffene mit Chorea Huntington ist dies sinnvoll, da diese Krankheit, je nachdem wieviele Triplettwiederholungen vorliegen, bereits bei Kleinkindern ausbrechen kann. Diesen, aber auch den anderen Menschen muss eine Therapie ermöglicht werden, da eine pharmakologische Behandlung meistens alleine nicht ausreicht.
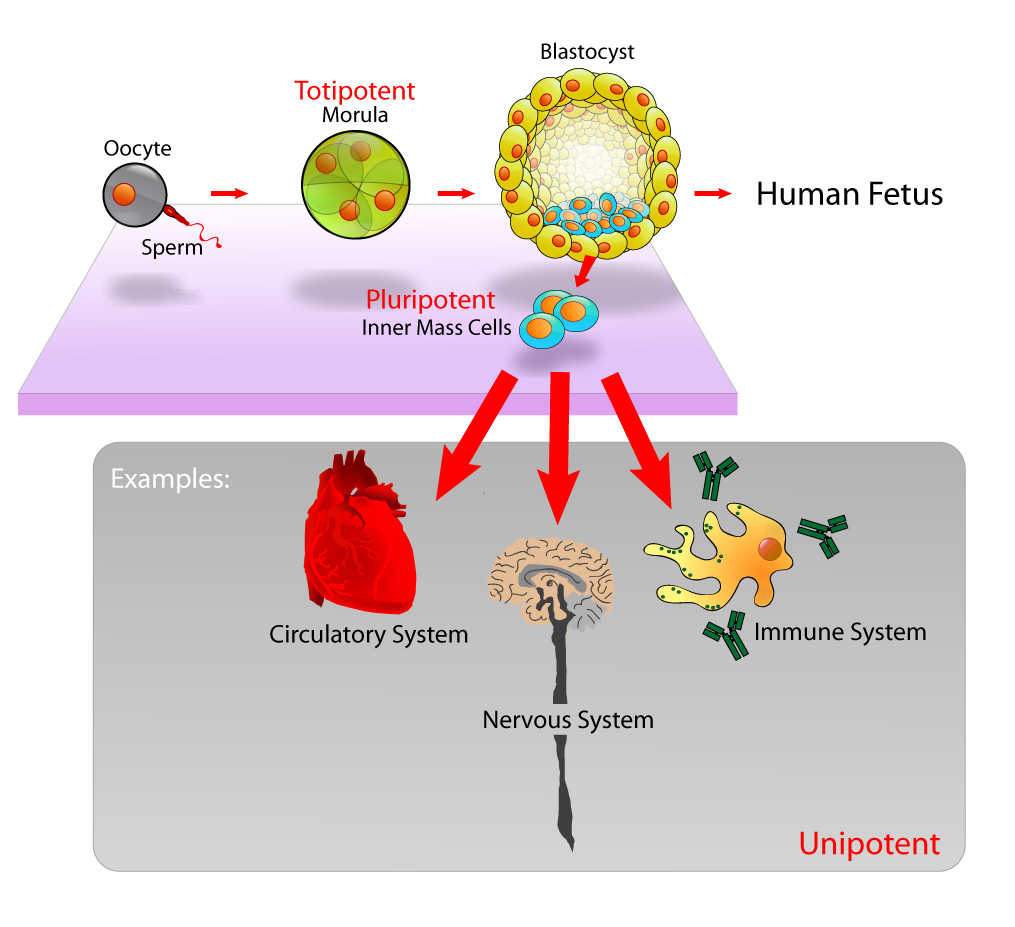
So viel zur Erklärung der Krankheiten, was kann man nun dagegen tun? Ich habe vorhin nicht umsonst Frankensteins Monster erwähnt, da die Behandlung durchaus so aussehen kann, dass der Mediziner dem Patienten eine Spritze mit Stammzellen in den Kopf jagt. Bevor dies aber der Fall ist, müssen diese Behandlungen in Tierversuchen überprüft werden und die Ergebnisse der letzten 10 Jahre lassen darauf deuten, dass die geschädigten Zellen in den drei oben erwähnten Krankheiten teilweise regeneriert werden konnten. Aber nicht nur das, erste Erfolge waren auch in Behandlungen der Multiplen Sklerose und der Ischämie des Gehirns, wobei es es sich um Durchblutungsstörungen handelt, zu verzeichnen. Zur Anwendung kommt hier vor allem ein bestimmter Typ von Stammzellen, den sogenannten embryonalen Stammzellen. Man kann diese aus embryonalem Gewebe gewinnen, welches aus der inneren Zellmasse eines 4-5 Tage alten Embryos entnommen wird. Diese Stammzellen besitzen im Gegensatz zu adulten Stammzellen eine besondere Charakteristik: Sie sind pluripotent und können sich so nahezu in jede andere Körperzelle verwandeln. Dies können adulte Stammzellen, die wir etwa in unserem Knochenmark finden, nicht. Hier wird nun die Wichtigkeit der Stammzellforschung offensichtlich.
Stammzellen stehen für die Behandlung also schon zur Verfügung. Es fehlen "nur noch" die letzten Schritte, die zu einer komerziellen Anwendung der Stammzelltherapie bei neurologischen Erkrankungen führen, getan werden müssen. Hier fällt besonders die Sicherstellung, dass die eingebrachten Stammzellen sich genau in die Zellen umwandeln, die sie ersetzen sollen, ins Auge. Zudem müssen sie sich korrekt in den Gewebeverbund integrieren. Nebenbei muss auch garantiert werden können, dass sich so Symptome lindern lassen, das allgemeine klinische Bild längerfristig verbessert wird und Nebeneffekte ausbleiben. Diese "nur noch" Schritte stellen also noch hohe Hürden dar, die mittlerweile aber angegangen wurden. In einigen klinische Studien z.B. wurden Chorea Huntington-Erkrankte mit fötalem Gewebe behandelt. Diese zeigten über die Zeit eine teilweise sehr gute Verbesserungen der Symptome, teils überhaupt keine. Zurückzuführen ist dieses augenscheinliche katastrophale Ergebnis der klinischen Studien auf das Problem, dass das implantierte fötale Gewebe sich wohl nicht richtig in das umliegende Gewebe integrieren konnte. Daraus kann man aber seine Lehren ziehen und die Durchführung der Therapien verbessern. Demnach müssen Protokolle zur gezielten Differenzierung und Integration ins Gewebe verbessert werden, was wohl heutzutage noch das größte Problem darstellt. Eine Möglichkeit für die gesteuerte Differenzierung in die richtigen Zelltypen wäre aber z.B. das Einsetzen von bestimmten genmanipulierten Viren, die den neu eingebrachten Zellen das richtige Schicksal zuweisen.
Um jetzt aber nicht alles schlecht zu reden und aussichtslos erscheinen zu lassen, muss man im Hinterkopf behalten, dass durchaus positive Ergebnisse produziert werden konnten. So wurden etwa bei 300-400 Parkinson-Erkrankten, die mit fötalen Zellen behandelt wurden, eine Verbesserung der Motorik festgestellt. Wichtig ist hier immer die Anwendung der geeignetsten Stammzellen, da man fetsgestellt hat, dass sich unterschiedliche Stammzelltypen unterschiedlich verhalten, wenn sie ins kranke Gewebe eingebracht werden.
Als abschließendes Fazit lässt sich sagen, dass Stammzelltherapien an Tiermodellen teilweise mit positiven Ergebnissen durchgeführt werden konnten. Erste klinische Studien mit Menschen bestätigen das, werfen aber weitere Fragen auf. So muss geklärt werden, welche Stammzellen sich für die Behandlung welcher Krankheit am besten eignen und wie man sie dazu bringt, dass sie sich in die Zelltypen differenzieren, die gewünscht werden. Sind diese Faktoren einmal geklärt, so sehe ich darin eine Möglichkeit, die Negativ-Ergebnisse aus den klinischen Studien wettzumachen, so dass der therapeutische Nutzen den Nebenwirkungen überwiegt.
Quellen:
- Progress and prospects: stem cells and neurological diseases, S. Gögel et al., Gene Therapy (2011) 18, 1–6; published online 30 September 2010, doi:10.1038/gt.2010.130
- Using human pluripotent stem cells to untangle neurodegenerative disease mechanisms, B. Malgrange et al., Cellular and Molecular Life Sciences Volume 68, Number 4, 635-649, DOI: 10.1007/s00018-010-0557-6
- Review Article: William J. Bowers, Xandra O. Breakefield and Miguel Sena-Esteves, Genetic Therapy for the Nervous System, Hum. Mol. Genet. (2011) first published online March 23, 2011, doi:10.1093/hmg/ddr110
- Jochen Graw, Genetik, 4., vollständig überarbeitete Auflage, ISBN-13 978-3-540-24096-9, Springer-Verlag

