Cytogenetik und die Genetik von Krebs: Methoden und Errungenschaften
BLOG: Enkapsis


1956 etablierten Tjio und Levan die Methode des Karyotyping und bestätigten, dass der Mensch 46 Chromosomen besitzt. Einige Jahre später wurden dann die ersten wichtigen Chromosomenveränderungen charakterisiert, die bei der Entstehung von Leukämie beobachtet wurden. Weitere wichtige Methoden zur Untersuchung von Chromosomen folgten in den 80er Jahren: Die Chromosomen-Bänderung mit der man die DNA durch bestimmte Behandlungen anfärbte, wobei je nach DNA-Zusammensetzung spezifische Bandenmuster entstanden. Die G-Banden-Färbung z.B. färbt dort Bereiche an, wo die DNA hauptsächlich aus Adenin und Thymin besteht. Heutzutage dient sie u.a. der Diagnose von Malaria. Nebenher gibt es auch noch die R-, C-, T- und Q-Banden-Färbung mit der sich unterschiedliche DNA-Zusammensetzungen auf den Chromosomen darstellen lassen, die man sich in einem Mikroskop anschauen kann. Die Darstellung der cytogenetischen Details wurde stets verfeinert und erweitert bis irgendwann das Auflösungsvermögen der Mikroskopie erreicht war. Es mussten neue Methoden her: mit der FISH wurde der Anfang gemacht und man konnte zum ersten mal Chromosomenmutationen sichtbar machen. Aber auch die Visualisierung von Translokationen bestimmter Bereiche war möglich. In den 90er Jahren wurde die array-CGH entwickelt. Es handelt sich dabei um einer der ersten DNA-Chips mit denen sich Veränderungen der DNA-Kopienzahl, entstanden durch den Zugewinn oder Verlust bestimmter Chromosomenregionen oder ganzer Chromosomen, sensitiv erkennen ließen.

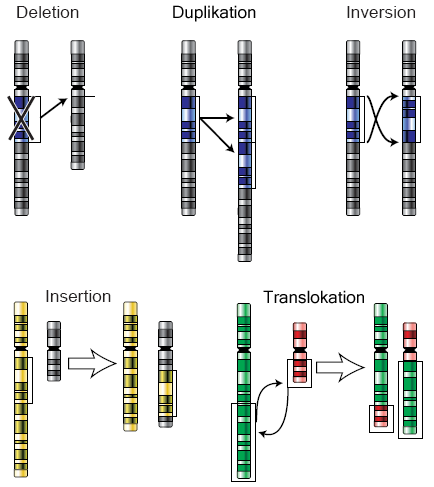
Cytogenetische Untersuchungen kommt eine sehr bedeutende Rolle in der Identifizierung von Chromosomen-Abnormalitäten zu. So kann man mit ihnen sogenannte Translokationen nachweisen. Darunter versteht man, dass nicht homologe Chromosomen untereinander Stücke austauschen und somit eine Neuanordnung von Genen entsteht, die in dieser Form Krebs auslösen kann. Sie machen den größten Teil von Chromosomen-Abnormalitäten in Leukämien und Lymphomen aus und durch deren Untersuchungen wurden schon unzählige krankheitsauslösende Neuanordnungen charakterisiert und tragen zum Verständnis bei, wie manche Krebsformen entstehen. Aber auch andere Chromosomenmutationen, wie z.B. Duplikationen, Deletionen, Inversionen und Insertionen sind mit cytogenetischen Untersuchungen nachweisbar, die ebenfalls zu einem Krankheitsbild beitragen. Was bei allen diesen Abnormalitäten zum Teil von statten geht, ist die Aktivierung von Onkogenen und die Inaktivierung von Tumor-Suppressorgenen. Die Folgen dabei sind fatal: wird ein Onkogen (auch Krebs-Gen genannt) aktiviert, so führt dies zu einem unkontrollierten Zellwachstum das in ein Tumorwachstum übergeht, da bestimmte Regulationsmechanismen von Zellen verstellt wurden und nun falsch ablaufen. Bei der chronischen myeloischen Leukämie enstehen durch Translokationen z.B. Fusions-Onkogene wie etwa BCR-ABL1. Bei Lungenkarzinomen ist das Fusions-Onkogen EML4-ALK bekannt. In beiden Fällen weiß man, dass Tyrosinkinasen aktiviert werden. Enzyme, die die Signalgebung von Zellen kontrollieren. Sie gelten bei der Krebsbehandlung neben vielen anderen als Therapie-Ansatzpunkt.
Derzeitige Trend in der Cytogenetik
Proteine werden in unserem Körper dadurch produziert, dass unsere DNA abgelesen und dieser Code in ein Protein umgewandelt wird. Dies geschieht in mehreren Schritten in denen natürlich eingegriffen werden kann. Moleküle die dies tun, sind sogenannte microRNAs (miRNAs). Es sind kleine einzelsträngige Moleküle, die das Ablesen von Genen und deren Übersetzung in Proteine ändern, stören und verhindern können. Es überrascht nicht, dass dies ebenfalls dazu beitragen kann, dass Krebs entstehen kann. Man stelle sich nur vor eines dieser microRNAs stört die Produktion eines Proteins, das von einem Tumorsuppressor-Gen stammt. Das Protein, welches dann normalerweise eine kaputte Zelle beseitigen würde, funktioniert nicht mehr richtig oder fehlt komplett und schon ist ein Faktor zur Krebsentstehung gegeben. MiroRNAs sind deswegen zurzeit ein populäres Forschungsobjekt, da die Bedeutung der miRNAs erst im letzten Jahrzehnt klar wurde und hilfreich für die Diagnose und Charakterisierung von Krebs sind.
Was hat die Cytogenetik also erreicht?
Die Kombination von cytogenetischen Methoden (FISH, PCR, SKY, Microarray, etc.) und molekularbiologischer Forschung hat bis heute wesentlich zum Verständnis der Krebsentstehung beigetragen. So konnten bisher viele Marker (Mutationen, wie z.B. Translokationen) identifiziert werden, die für bestimmte Krebsarten charakteristisch sind. Findet man diese Marker durch systematische Analyse der Gene und Chromosomen, so können sie als Ansatzpunkte für Therapien dienen.
Take-Home-Messages
1. Chromosomenveränderungen, insbesondere Translokationen, sind Schlüsselelemente zur Diagnose von Krebs.
2. Cytogenetische Untersuchungen sind bei Kebspatienten notwendig, um so Chromosomenmutationen und Genmutationen aufzudecken, die die Krankheit auslösen und die ihre Aggressivität ausmachen.
3. Die Untersuchung von Chromosomenveränderungen tragen dazu bei "kaputte" Gene zu identifizieren.
Literatur:
- Cytogenetics and genetics of human cancer: methods and accomplishments; Avery A. Sandberg, Aurelia M. Meloni-Ehrig; Cancer genetics and cytogenetics 1 December 2010 (volume 203 issue 2 Pages 102-126 DOI: 10.1016/j.cancergencyto.2010.10.004)

