Humane embryonale Stammzellen aus unbefruchteten Eizellen – Ein Ausweg?
BLOG: Die Sankore Schriften

Bei der Zellersatztherapie differenzieren Wissenschaftler Stammzellen in bestimmte Zelltypen, um alte kranke Zellen durch neue gesunde zu ersetzen. Viele Neurologen träumen davon mit diesem Ansatz die Parkinson-Krankheit zu heilen: Neue gesunde, im Labor hergestellte, Nervenzellen nehmen den Platz der geschädigten Dopamin produzierenden Nervenzellen in der Pars compacta der Substantia nigra des Patienten ein.
Embryonale Stammzellen eignen sich am besten für die Zellersatztherapie, weil sie pluripotent sind: Sie lassen sich zu jeglichem Zelltyp eines Organismus differenzieren und entwickeln zahlreiche Gewebe.
Das Embryonenschutzgesetz
Embryonale Stammzellen gewinnt man aus einem – Du hast richtig geraten – Embryo und damit sind wir beim ersten und ethisch wichtigsten Problem der Zellersatztherapie. Der deutsche Gesetzgeber sieht die Zellen des Embryos als besonders schützenswert an, weil sich aus Ihnen später ein Mensch entwickelt. Das Embryonenschutzgesetz hat zum Ziel, das menschliche Leben von seinem Beginn an zu schützen.
In § 8 wird definiert, dass als Embryo im Sinne des Gesetzes bereits die befruchtete, entwicklungsfähige Eizelle angesehen wird. Entwicklungsfähig ist eine Eizelle innerhalb von 24 Stunden nach der Kernverschmelzung (§ 8 Abs. 1). Außerdem gilt jede Zelle, die man einem Embryo entnimmt, selber als Embryo, wenn sie sich selbst zu einem vollständigen Individuum entwickeln könnte (Totipotenz). Ob das auf humane embryonale Stammzellen zutrifft ist wissenschaftlich umstritten und lässt sich aus ethischen Gründen auch schlecht feststellen. Hübner et al. [1] zeigten, dass embryonale Stammzellen der Maus sich in vitro nicht nur zu Körperzellen sondern auch zu Eizellen und extraembryonalen Zellen entwickeln können. Toyooka Y et al. [2] zeigten, dass sich embryonale Stammzellen der Maus in vitro auch zu Spermienvorstufen differenzieren können, die nach Transplantation in den Hoden zu Spermien heranreifen.
In § 2 geht es um die missbräuchliche Verwendung des menschlichen Embryos. So wird die Weiterbehandlung eines Embryos außerhalb des Mutterleibs nur erlaubt, wenn der Embryo anschließend der Mutter eingepflanzt wird (§ 2 Abs. 2).
Cruz Villalón, Generalanwalt des Europäischen Gerichtshofs (EuGH), definiert jedoch einschränkend das “eine Eizelle, die ohne Befruchtung zur Weiterentwicklung angeregt worden ist” und die “nicht fähig ist, sich zu einem Menschen zu entwickeln, nicht als menschlicher Embryo angesehen werden kann”.
Er zeigte damit einen Weg auf wie diese ethische und rechtliche Hürde der embryonalen Stammzellgewinnung umgangen werden kann. Um diesen Weg zu verstehen müssen wir uns mit Parthenogenese beschäftigen.
Parthenogenese von humanen Eizellen
Bei der Parthenogenese werden Eizellen ohne Befruchtung, also unabhängig vom Spermien aktiviert. Man nennt diese Eizellen Parthenote. Parthenote teilen sich und bilden einen neuen Organismus. Wirbellose Tierarten wie Bienen, Rädertiere, Wasserflöhe, Schlupfwespen und Blattläuse bedienen sich gelegentlich dieser eingeschlechtlichen Fortpflanzungsform.
Parthenote von Säugetieren sind nicht lebensfähig. Eizellen von Mäusen oder Kaninchen, die durch chemische Reize angeregt wurden, sich zu teilen, unterscheiden sich in den ersten Entwicklungstagen nicht von befruchteten Eizellen. Sie enthalten auch pluripotente embryonale Stammzellen, stoppen aber in der Entwicklung und sterben nach etwa 10 Tagen ab [3-6]. Embryologen führen den Tod darauf zurück, dass das paternale Imprinting der Gene (unter anderem Methylierungsmuster) in der Zygote offenbar eine Bedeutung für die Entwicklung hat, die bisher nur unvollkommen verstanden ist.
2004 aktivierten Nina Rogers vom University College London und ihre Kollegen von der Cardiff University humane Eizellen parthenogenetisch, indem sie die RNA des Spermienproteins Phospholipase Czeta in die Zellen injizierten [7]. Einige der Zellen teilten sich bis zum Blastozystenstadium. Bislang ist es aber noch nicht gelungen, die innere Zellmasse der Blastozysten weiter zu kultivieren und daraus embryonale Stammzellen gewinnen.
Wenn das gelingt, wäre folgendes denkbar: Frauen mit chronischen Erkrankungen, wie z. B. Typ-1-Diabetes, werden Eizellen entnommen um daraus immuntolerante insulinproduzierende Betazellen der Langerhansschen Inseln der Bauchspeicheldrüse herzustellen. Rechtlich könnte dann ein solcher Vorgang mit einer Eigenblutspende vor einer Operation oder der Gewinnung von Blutstammzellen aus dem Knochenmark verglichen werden.
Weiterführende Literatur
What are stem cells? – An short educational film by the Irish Stem Cell Foundation
Creation of human embryonic stem cell lines
First embryonic stem cell therapy safety trial in Asian patients
1. Hübner K, Fuhrmann G, Christenson LK, Kehler J, Reinbold R, De La Fuente R, Wood J, Strauss III JF, Boiani M, Schöler HR (2003) Derivation of oocytes from mouse embryonic stem cells. Science, 300, 1251–1256.
2. Toyooka Y, Tsunekawa N, Akasu R, Noce T (2003) Embryonic stem cells can form germ cells in vitro. USA: Proc Natl Acad Sci, 100, 11457–11462.
3. Surani MA , Barton SC (1983) Development of gynogenetic eggs in the mouse: implications for parthenogenetic embryos. Science, 222, 4627, 1034-1036.
4. Surani MA, Barton SC, Norris ML (1984) Development of reconstituted mouse eggs suggests imprinting of the genome during gametogenesis. Nature, 308, 5959, 548-550.
5. Surani MA, Kothary R, Allen ND, Singh PB, Fundele R, Ferguson-Smith AC, Barton SC (1990) Genome imprinting and development in the mouse. Dev Suppl, 89-98.
6. McGrath J, Solter D (1984) Completion of mouse embryogenesis requires both the maternal and paternal genomes. Cell, 37, 1, 179-183.
Bildnachweis
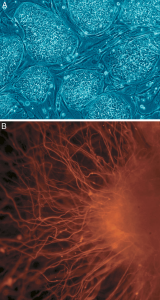
Beschreibung: (A) Humane embryonale Stammzellen (hESCs); (B) Nervenzellen, die aus humanen embryonalen Stammzellen hergestellt wurden
Urheber: Nissim Benvenisty
Datum der Veröffentlichung: 12.7.2005
Lizenz: This file is licensed under the Creative Commons Attribution 2.5 Generic license.


Pingback:[SciLogs] Humane embryonale Stammzellen aus unbefruchteten Eizellen – Ein Ausweg? | netzlesen.de