Genexpression im Gehirn live beobachten!
BLOG: Die Sankore Schriften

Um die Expression eines bestimmten Gens im Gehirn der Maus unter verschiedenen Bedingungen zu untersuchen, wird die Maus nach dem Experiment normalerweise getötet, um die spezifische mRNA dieses Gens aus dem Gehirn zu isolieren. Philip Liu und sein Forscherteam in Boston, Massachusetts gelang es die spezifische Genexpression im Maushirn direkt im lebenden Tier zu beobachten.
Dazu kombinierten sie die In situ Hybridisierung, eine zellbiologische Methode, mit der Magnetresonanztomografie (MRT), einem bildgebenden Verfahren.
Die Hochzeit von In Situ Hybridisierung und Magnetresonanztomografie (MRT)
Mit der In situ Hybridisierung weist man eine spezifische mRNA- oder DNA-Sequenz vor Ort (in situ), das heißt in der Zelle nach. Diese Technik lässt sich in der Zellkultur oder im Gewebedünnschnitt anwenden. Dabei wird einzelsträngige RNA, die mit einer Markierung versehen wurde, als sogenannte Sonde eingesetzt. Wichtig ist, dass die Sonde die komplementäre Sequenz der Ziel-mRNA aufweist. Die Sonde kann dann spezifisch an die Ziel-mRNA binden. Diese Bindung eines Nukleinsäurestranges an einen komplementären Strang nennt man Hybridisierung.
Bei der Magnetresonanztomografie wird der Patient einem starkem Magnetfeld und kurzzeitig auch Radiowellen ausgesetzt. Durch das Magnetfeld gehen die Wasserstoffkerne des menschlichen Körpers von einem energiearmen in einen energiereichen Zustand über. Durch die Radiowellen geraten die Atome geraten in Schwingung. Schaltet man die Radiostrahlung wieder aus, so gehen die Atomkerne wieder in den energiearmen Zustand zurück. Dabei senden sie Radiowellen aus, die durch hochempfindliche Antennen gemessen werden können. Ein Computer berechnet aus den Signalen ein Schnittbild durch den Körper. Diese Schnittbilder werden später zu einem dreidimensionalen Bild zusammengesetzt.
In dem hier beschriebenen Experiment wiesen die Wissenschaftler die Expression des Onkogens c-fos in verschiedenen Hirnregionen nach. Die Sonde für c-fos mRNA markierten sie doppelt mit Biotin und einem Fluoreszenzfarbstoff. Als Sender der Radiosignale für das MRT dienten hier statt der Wasserstoffkerne, superparamagnetische Nanopartikel aus Eisenoxid sogenannte SPIONS (Superparamagnetic Iron Oxide Nanoparticles). Die SPIONS haben nur magnetische Eigenschaften wenn sie sich in einem Magnetfeld befinden und aufgrund ihrer Größe, tausendmal kleiner als Nervenzellen, werden sie von den Zellen gut aufgenommen. Zusätzlich koppelten die Forscher Avidin an die SPIONS.
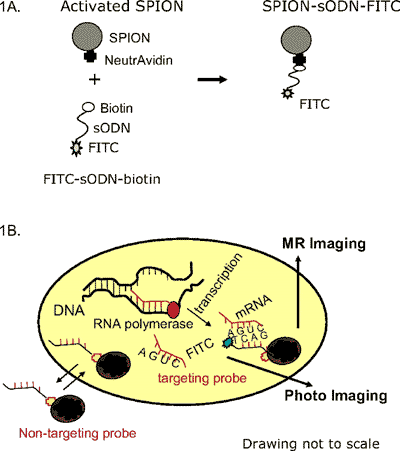
1A zeigt das Design der Sonde und des SPIONS 1B zeigt schematisch wie eine zelluläre mRNA mit Hilfe der Sonde und des SPIONS lokalisiert werden kann
Um nun die SPIONS und die Sonden zusammenzubringen nutzen die Wissenschaftler die Affinität von Avidin zu Biotin. Avidin ist ein aus Hühnereiweiß gewonnenes Glykoprotein, das in den Zellen als Homotetramer vorliegt und vier Bindungsstellen für Biotin, ein wasserlösliches Vitamin, hat. Avidin wird heutzutage in reinerer Form, gentechnisch hergestellt. Diese Variante des Avidins nennt man Streptavidin und wird aus dem Bakterium Streptomyces avidinii isoliert. Natürlich muss man bei dieser Methode darauf achten, falls endogenes Biotin im Gewebe vorhanden ist, dieses zu blockieren, da es sonst unspezifische Bindungen herbeiführt.
In dem Experiment untersuchten die Forscher zwei Gruppen von Mäusen. Die eine Gruppe wurde mit einer Kochsalzlösung behandelt, die andere mit Amphetamin. Amphetamin induziert die Expression von c-Fos im Nucleus accumbens, Striatum und Cingulate. Sie injizierten die Sonden in die linken Ventrikel der Mäuse und schauten in der T2-MRT, in welchen Hirnregionen sich Signale zeigten. Zusätzlich verglichen sie die Signalstärke in den beiden Gruppen. In beiden Gruppen fanden sie Signale im Nucleus accumbens, Striatum, Cingulate, prälimbischen und infralimbischen Cortex. In der mit Amphetamin-behandelten Gruppe waren die Signale in all diesen Hirnregionen stärker als in der mit Salzlösung behandelten Gruppe. Ein Traum der Wissenschaftler ist es nun diese Technik weiter zu entwickeln und sie für die Diagnose psychiatrischer und neurologischer Krankheiten beim Menschen einzusetzen.
Weiterführende Literatur
Bildnachweis
Figure 1 aus dem oben zitierten Paper
Liu, C., Kim, Y., Ren, J., Eichler, F., Rosen, B., & Liu, P. (2007). Imaging Cerebral Gene Transcripts in Live Animals Journal of Neuroscience, 27 (3), 713-722 DOI: 10.1523/JNEUROSCI.4660-06.2007

