Größensortierung von Biomolekülen und ein Hilferuf
BLOG: Detritus

Ich habe wohl schon hunderte Gele gegossen und laufen lassen – die Elektrophorese von Biomolekülen ist für mich die Labor-Standardmethode schlechthin. Trotzdem sorgt sie immer wieder für Überraschungen. Ein Rätsel des Laboralltags, das ich bisher noch nicht gelöst habe, gibt’s am Ende dieses Posts.
Das grundlegende Prinzip der Elektrophorese (darin steckt griech. phoresis, „getragen werden“), das ist recht einfach. Geladene Teilchen – wie etwa DNA – wandern im elektrischen Feld: positiv geladene Teilchen zur negativ geladenen Kathode, und negativ geladene Teilchen zur positiv geladenen Anode. Stellt man den Teilchen etwas in den Weg, etwa ein molekulares Sieb in Form eines Gels, dann werden sie in ihrer Bewegung behindert.
Je größer das Molekül, desto öfter bleibt es in den Poren des Gels „hängen“ und desto langsamer wandert es auch. Kleinere Teilchen wandern demnach schneller. So kommen auch die berühmten Bilder von „genetischen Fingerabdrücken“ zustande – jeder Streifen („Bande“) steht für eine Menge DNA-Moleküle einer bestimmten Länge. Je intensiver die Bande, desto mehr DNA enthält sie.
Der blaue Farbstoff, der sich dort bewegt, dient nur dazu, die meist farblose Probe einfacher pipettierbar zu machen. Die Proteine und eigentlichen Subjekte des Experiments muss man später separat färben. Wenn man aber genau hinschaut, dann sieht man am rechten Rand eine schmale Reihe aus farbigen Streifen, die sich langsam auftrennen. Das sind bereits vorgefärbte Proteine, die man als Standard einsetzt, als Vergleich zu seinen unbekannten Proteinen.
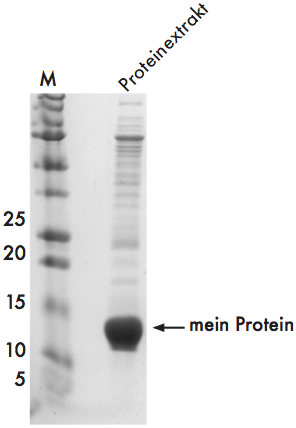
In dem obigen Schwarzweißbild sieht man links die Leiter aus Standardproteinen, und rechts einen Proteinextrakt mit allerhand Verunreinigungen und meinem Protein, das in so hoher Konzentration vorliegt, dass die Bande über ihre Grenzen quillt. Anhand der Standardleiter links kann ich sehen, dass es etwa 11 Kilo-Dalton groß ist. Das ist jetzt kein besonders schönes Beispiel, aber wie es auch richtig schief gehen kann, demonstriert die Hall of Shame der Proteingele von David R. Caprette.
Und folgendes Phänomen hatte ich bei einem Gel, das eine Woche im Kühlschrank lag:
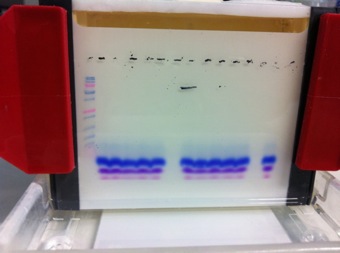
Gleich drei Farbstoffbanden! Wie kommt das? Bislang konnte mir niemand erklären, woher diese zusätzlichen Banden, die schneller laufen als der 2-kDa-Standard, herkommen.
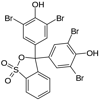
In dem Video ganz oben sieht man, dass dort ebenfalls ganz schwach eine geisterhafte Bande mitläuft, etwas schneller als das eigentlich blaue Bromphenolblau (siehe rechts). Die Farbe von Bromphenolblau ist abhängig vom pH-Wert: Im sauren Milieu ist er gelb, im neutralen und basischen Bereich ist er blau. Die schneller laufenden Banden könnten unterschiedlich geladenen Spezies des Bromphenolblaus darstellen, das passt aber nicht mit dem Farbumschlag in Richtung gelb bei stärkerer Protonierung. Von lila und rosa habe ich auch nirgends gelesen.
Wer weiß, was die zusätzlichen Banden bedeuten?



Kosten?
Magst du mir für meine Liste Geld und Wissenschaft: 14 Größenordnungen sagen, wieviel Gelelektrophorese kostet? Sowohl der Apparat als auch ein einzelnes Gel?
Kosten
Hier ist ein ähnliches Gerät, aber für liegende Agarose-Gele und DNA, beschrieben:
https://scilogs.spektrum.de/…ielf-ltigung-in-der-k-che
Kosten von $498 + $199:
http://www.pearlbiotech.com/buy/
Verunreinigung
Besonders alte Lösungen von Bromphenolblau enthalten viel von dieser violetten Verbindung.
Die meisten Probeauftragspuffer enthalten reduzierende SH-Verbindungen, die vielleicht das Bromphenolblau modifizieren, wenn sie lange Zeit dafür haben, oder wenn sie damit erwärmt werden.
Oder das Bromphenolblau oxidiert schon vorher ein wenig, was die höhere Elektro-Negativität erklären würde.
Während der Elektrophorese verändert sich das Bromphenolblau bestimmt nicht mehr, denn beide Banden sind klar von einander getrennt.
Was man vom Bromphenolblau und seinem Derivat hier sieht, ist aber seine Salzform, die oberhalb von pH 4,6 auftritt.
Bild:
http://www.chemicalbook.com/…IF%5C33551-92-7.gif
Man könnte die violette Bande herauslösen, und ein Spektrum von ihr machen.
Noch viel besser wäre natürlich ein NMR dieser Substanz.
Vielleicht könnte man einen Chemiestudenten darauf ansetzen.
—–
Meine stolzen Werke:
Eukaryotischer Elongationsfaktor 1:
http://members.chello.at/….bednarik/NATSDS2D.jpg
Dichtegradientenelektrophorese (1972):
Ein vergilbtes Bild:
http://members.chello.at/…k/DSCM1962-DGE-BPB.JPG
Vier bessere Bilder:
http://de.wikipedia.org/…radientenelektrophorese
Der Artikel dazu:
http://onlinelibrary.wiley.com/…5F67F358F.d01t02
@ Karl:
Danke für deinen Input! Ganz frisch ist der Puffer nicht mehr, also wäre es gut möglich, dass das Bromphenolblau inzwischen modifiziert wurde. NMR-Spektrometer haben wir hier zu Genüge, allerdings habe ich die Banden nicht ausgeschnitten, sondern das Gel fixiert und gefärbt. Und reproduzieren konnte ich es bislang nicht mehr, das obige Gel hatte wohl durch einen Fehler meinerseits eine geringere Porengröße – oder ich habe aus versehen einen anderen Puffer gegriffen.
@ Markus:
Die von Krl oben genannten horizontal laufenden Gele sind billiger. Für die SDS-PAGE braucht man außerdem noch Gießstation, Glasplatten, Spacer und die Reagenzien für die Gelherstellung (beim Agarosegel ist das ja nur Agarose).
Die Kammer, in der so ein Minigel läuft, kostet so um die 1000 EUR. Die Spannungsquelle kostet nochmal so etwa 250 EUR IIRC. Dazu kommen die Verbrauchsmaterialien und der Proteinstandard, außerdem kann man Puffer etc. auch kaufen.
Die Kosten könnte ich bei Gelegenheit mal überschlagen, sind aber je Gel eher gering. Gekaufte und vorgegossene Gele kosten so etwa 20 EUR, glaube ich (kommt wahrscheinlich auf den Typ Gel an).
Vielleicht lohnt es sich, bei http://www.carl-roth.de/ zu stöbern, ich habe dafür heute leider keine Zeit.
Beim recht günstigen Anbieter Roth kostet das Ganze im Komplettset 730 € plus Netzteil, ca 500 €:
http://www.carlroth.com/…ang=de-de&market=DE
mehrere Farbstoffe
Soviel ich weiß hat der Probenpuffer ja manchmal drei Farbstoffe: Bromphenolblau, Xylencyanol, Orange G. Der pH-Wert ändert sich ja mit der Temperatur und nach einer Woche im Kühlschrank bei 4 C Grad kann natürlich einiges geschehen. Ich glaube auch, das nach dem das Gel gelaufen ist die lokale H+-Konzentration an der Anode wegen der Abstoßung geringer ist als an der Kathode.
Also intuitiv
stimme ich Karl Bednarik zu: Wenn der Farbstoff tatsächlich Bromphenolblau ist (d.h. klassisch), dann sind da zwei Phenolische OH-Gruppen drin, die oxidiert werden können können. Das erklärt auch zwanglos weshalb es drei Banden sind.
Hast du das Gel noch? Dann kannst du es ja mal extrahieren und n NMR von allen drei Banden machen lassen.
Gießstation
Eine Gießstation kann man sich ersparen, wenn man vor dem Gießen des Trenngels in den unteren 2 cm der Glasplatten einen Gelstopfen aushärten lässt.
Bei einfachen, vertikalen Gelapparaturen mit einem Anodenpufferbehälter, der nach vorne gerichtet ist, neigt man dazu das vollständig zusammen gebaute Gerät um 45 ° nach hinten.
Dadurch entsteht ein keilförmiger Gelstopfen, der beim Trennlauf dann im Anodenpuffer liegt.
—–
Diese violette Verunreinigung des Bromphenolblaus hatte ich immer und bei allen Arten von Gelen.
Wenn der Anodenpuffer übersäuert und unter pH 4,6 geht, dann wird die Bromphenolblaubande am unteren Rand des Gels gelb.
OK, jetzt erst gelesen…
Wenn du nicht was ganz exotisches mit dem Gel gemacht hast, sollte die Fixierung für so ne simple Chemikalie wie das Phthalein keinen Unterschied machen, IMO.
Hallo Lars Fischer,
wenn man ein Gel fixiert und färbt, dann diffundiert der Farbstoff hinein, und das Bromphenolblau mitsamt allen kleinen Molekülen diffundiert heraus.
Spannende Theorie, klingt plausibel. Aber passt das mit den Bandenpositionen zusammen?
Oxidiere mal ein Aliquot & lass es neben einer frischen Lösung laufen.
Oxidation
Die Oxidation von phenolischen Verbindungen geht in den meisten Fällen mit der Salzform im neutralen und basischen pH-Bereich schneller vor sich, als mit der freien Säure, das ist auch bei den Foto-Entwicklern so.
Die Anwesenheit von SH-Verbindungen sollte aber eine Oxidation verhindern, so lange die SH-Verbindungen nicht schon selbst oxidiert worden sind.
—–
Polyacrylamid-Gelelektrophorese-Tricks:
Wenn man an Stelle von N,N’-Methylenbisacrylamid N,N’-Diallyltartardiamid verwendet, dann kann man das Gel nach dem Trennlauf mit Natriumperiodatlösung durch Glykolspaltung wieder auflösen, was die Untersuchung der getrennten Substanzen erleichtert. Das gilt zumindest für die Radioaktivität, und eher weniger für die biologische Aktivität.
Wenn man an Stelle von Ammoniumperoxodisulfat Riboflavin verwendet, dann kann man mit Hilfe von hellem, blau-violettem Licht den Zeitpunkt der Polymerisation selbst bestimmen, was einen größeren zeitlichen Spielraum für das Gießen des Gels erlaubt.
Nativ-Gelelektrophorese-Tricks:
Um die bei der Aushärtungsreaktion des Polyacrylamidgels zugesetzten und entstehenden, eventuell störenden, Stoffe zu entfernen, und um die Ionen des Laufpuffers einwandern zu lassen, kann man das Gel vor dem Trennlauf eine Zeit lang ohne die zu trennende Probe elektrisch laufen lassen, und danach den Laufpuffer erneuern.
Einige Proteine benötigen zu ihrem Schutz eine geringe Konzentration an reduzierenden Verbindungen, wie zum Beispiel Dithioerythrit. Solche Verbindungen können die Aushärtungsreaktion des Polyacrylamidgels entweder stören, oder selbst bei der Aushärtungsreaktion des Polyacrylamidgels zerstört werden. Das hinein Diffundieren von elektrisch neutralen Molekülen in das Gel würde sehr lange dauern. Deshalb kann man an Stelle der sonst üblichen elektrisch neutralen reduzierenden Verbindungen Cystein elektrisch einwandern lassen. Der isoelektrische Punkt von Cystein liegt bei einem pH-Wert von 5,02. Bei diesem pH-Wert bringt Cystein keine Vorteile.
Bei vielen für die Nativ-Gelelektrophorese erforderlichen Puffersystemen entstehen an der Kathode (- Pol) stark basische und stark reduzierende Verbindungen, und an der Anode (+ Pol) stark saure und stark oxidierende Verbindungen, wie zum Beispiel Hypochlorite. Um die Probe davor zu schützen, sollte man mehrere Elektrodenpuffergefäße verwenden, die durch mit Elektrodenpuffer gefüllte Stromschlüssel verbunden sind, so wie es im oberen Teil des Bildes gezeigt wird, und zumindest den pH-Wert dieser Puffergefäße regelmäßig überprüfen.
Bild:
http://members.chello.at/karl.bednarik/DGE-Z.PNG
@fatmike
Ein Problem ist ja, dass das Gel selbst auch anders war, als alle vorher laufenden Gele: es lief langsamer und hatte eine höhere Trennschärfe. Möglicherweise habe ich auch einfach einen falschen Puffer gegriffen, und damit die bessere Trennung prvoziert. (Ich habe noch ein HEPES-Puffersystem für gekaufte Gradientengele zu Hand.) Ich werde mal ein normales Lämmli-Gel mit dem anderen Puffer laufen lassen, vielleicht hat es ja einen Effekt 🙂
Das mit der Oxidation ist, wie Karl schreibt, eher unwahrscheinlich, denn ich habe recht viel DTT im Puffer. Der ist auch immer eingefroren (-20°C). Vielleicht oxidiert aber auch schon das pulverisierte Bromphenolblau in der (uralten) Vorratsflasche?
@Karl
Ich habe, wie gerade geschrieben, eigentlich ausreichend DTT im Puffer.
Danke für die Elektrophorese-Tipps, einige kannte ich schon 🙂
Letztens auch den Tipp gesagt bekommen, das Sammelgel mit etwas Bromphenolblau zu gießen, dann sieht man die Taschen besser und muss sie sich nicht anzeichnen (das mache ich immer).
Was sagst du dazu, (besonders Schägger&Jagow-Gele) über-Nacht im Kühlschrank „auspolymerisieren“ zu lassen? Einige sind der Meinung, dass die Gele dann besser „performen“ würden, ich habe so einen Unterschied noch nicht festgestellt.
Den Teil mit den Pufferbehältern verstehe ich nicht. Meinst du, dass innerhalb der kurzen Laufzeit genug schädliche Stoffe entstehen könnten? Der Puffer kommt bei mir nach dem Lauf immer weg, wiederverwenden tu’ ich den nicht!
Hallo Martin Ballaschk,
rein theoretisch würde ich sagen, dass die Polymerisation in der Wärme vollständiger (und natürlich schneller) vor sich geht.
Aus diesem Grund kam ich nie auf die Idee, bei der Polymerisation zu kühlen.
Bei Nativ-Gelen ist es aber günstig, während des Trennlaufes zu kühlen, damit die Proteine nicht kaputt gehen.
Die Elektrodenpuffertrennung ist nur bei Nativ-Gelen notwendig, um die Proteine vor den elektrolytischen Zersetzungsprodukten zu schützen.
Bei SDS-Gelen benötigt man keine Elektrodenpuffertrennung, solange sich das Bromphenolblau nach dem Trennlauf am unteren Ende des Gels nicht in die Richtung zum gelbgrün verfärbt.
Es kann aber nichts schaden, die pH-Werte der beiden Elektrodenpuffer nach dem Trennlauf zu bestimmen (mit den Teststäbchen von Merck).
Natürlich sollte man die Elektrodenpuffer niemals mehrfach verwenden.
Als elektrolytische Zersetzungsprodukte kommen an der Kathode (-) vor:
Wasserstoff, Alkalihydroxide, freie Basen der Puffersubstanzen, und Reaktionsprodukte dieser Substanzen.
An der Anhode (+):
Sauerstoff, Chlor, Salzsäure, Unterchlorige Säure, freie Säuren der Puffersubstanzen, und Reaktionsprodukte dieser Substanzen.
—
Mein Kollege R. H. sagte immer:
“Nicht verwechseln, rot ist blau, und plus ist minus.”
Sammelgel
Wenn man das Sammelgel zusammen mit Bromphenolblau polymerisiert, dann kann das Bromphenolblau durch die oxidierende Komponente des Radikalbildners oxidiert werden.
Normalerweise ist das Ammoniumperoxodisulfat (APS), oder Riboflavin mit Luftsauerstoff, während die reduzierende Komponente zumeist Tetramethylethylendiamin (TEMED) ist.
Die Salzform des Bromphenolblaus hat nur noch eine phenolische OH-Gruppe, die freie Säure hat aber zwei.
Sammelgel zwei
Man könnte auch das Sammelgel nach seiner Polymerisation mit einer kleineren Menge von Elektrodenpuffer, der Bromphenolblau enthält, es kann auch Probenauftragspuffer sein, überschichten, und eine halbe Stunde stehen lassen.
Danach entfernt man den Bromphenolblau enthaltenden Elektrodenpuffer, und ersetzt ihn durch den normalen Elektrodenpuffer.
Nun müsste man besonders die Konturen des Sammelgels deutlich erkennen können, weil dort am meisten Bromphenolblau eindiffundiert ist.
Warum bin ich nicht schon vor 40 Jahren auf diese Idee gekommen?
Hm, aber 30 min warten ist länger, als 1 min Taschen anzeichnen. Eigentlich reicht ja auch eine starke lichtquelle, im richtigen Winkel auf das Gel gerichtet, um die Konturen zu erkennen.
Ich werde trotzdem als erstes versuchen, Bromphenolblau zum Sammelgel zu geben, es reicht ja eine minimale Menge.
Und separat etwas APS-oxidiertes Bromphenolblau laufen werde ich auch, vielleicht ist das dann komplett violett-rot 🙂
sichtbare taschen
.. einfach vor dem auftragen der proben wenige mikroliter probenpuffer oberhalb der taschen verteilen – bromphenolblau sinkt ab und zeichnet die konturen der taschen perfekt nach.