Personalisierte Medizin und Genomsequenzierungen – Medizin im Wandel
BLOG: Bierologie

Seitdem die ersten Nobelpreise vergeben wurden haben wohl fast alle Disziplinen, die mit einem solchen Preis beehrt werden, einen ungeheuren Wandel durchgemacht. Für mich ist die Kategorie Physiologie oder Medizin, meist schlicht „Medizinnobelpreis“ genannt, dabei besonders spannend. Nicht nur, weil mir die Kategorie als Biologe am nächsten ist, sondern auch, weil sie oft jene Ergebnisse prämiert, die vermutlich am unmittelbarsten in das Leben vieler Menschen eingreift.
1901 bekam Emil von Behring den Preis, für seine Arbeit an dem, was wir heute als Impfstoffe kennen und was seitdem viele Krankheiten zumindest in Industrieländern fast komplett ausgerottet hat. Karl Landsteiner im Jahre 1930 für die Entdeckung der Blutgruppen, ohne die es keine oft benötigten Bluttransfusionen gäbe. 1945 war Alexander Flemming für die Entdeckung des Penicillins und damit der Antibiotika, deren Entdeckung (auch wenn multiresistente Erreger heutzutage auf dem Vormarsch sind) ebenfalls so manchem das Leben gerettet hat, an der Reihe.
Vielleicht weniger unmittelbar, aber deshalb nicht weniger wichtig, sind die Entdeckungen von Watson, Crick und Wilkins, die den Preis 1962 für die Entdeckung der DNA-Struktur verliehen bekommen haben oder von Holley, Khorana und Nirenberg, die mit an der Entschlüsselung des genetischen Codes beteiligt waren und dafür 1968 ausgezeichnet wurden. Damit haben sie die Voraussetzungen dafür geschaffen, dass die moderne Medizin sich in der Lage sieht Erbkrankheiten nicht nur zu entdecken, sondern auch die Auswirkungen von einzelnen Mutationen versteht und damit auch in immer stärkerem Maß etwas gegen entsprechende Krankheiten unternehmen kann. Daran nicht weniger mitverantwortlich ist Frederick Sanger, der 1980 den Nobelpreis – allerdings in der Disziplin Chemie – für seine Arbeit an der DNA-Sequenzierung bekam und damit erstmals einen wirklichen Einblick in unsere genetischen Grundlagen ermöglichte. Und wohl keiner der Genannten hätte zu träumen gewagt, welchen Siegeszug die Genetik bereits jetzt in der Medizin antritt.
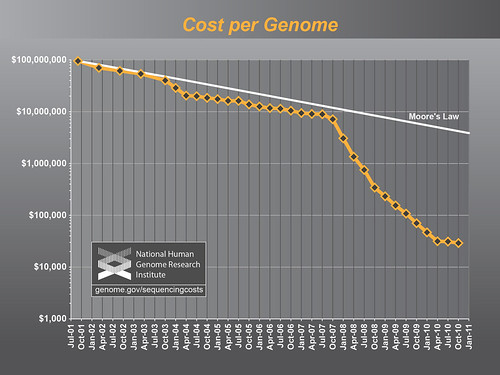
Als das Human Genome Project im Jahre 2000 das erste komplett sequenzierte menschliche Genom vorstellte, hatte das Projekt bereits über 10 Jahre mit Wissenschaftlern auf der ganzen Welt daran gearbeitet. Und gute 3 Milliarden US Dollar gekostet. Mehr als 10 Jahre nach der Veröffentlichung dieser ersten Version sind zwar noch nicht alle Krankheiten besiegt, trotzdem wurde damit ein Meilenstein in der Medizingeschichte gelegt. Denn das erste sequenzierte Genom sollte nur der Anfang sein. Im Jahr 2007 wurden die Genome von James Watson und Craig Venter veröffentlicht. Geschätzter Zeitaufwand und Kostenpunkt pro Genom: 2 Monate und 3 Millionen US Dollar. Aber auch dabei sollte es nicht bleiben, denn sowohl die benötigte Zeit, als auch die Kosten, sinken beständig weiter.
Gordon Moore formulierte 1965 das nach ihm benannte Gesetz, dass sich die Komplexität integrierter Schaltkreise mit minimalen Komponentenkosten alle 18 Monate verdopple. Oder anders ausgedrückt: Alle 18 Monate halbieren sich die Kosten für eine konstante Rechenleistung. Das National Human Genome Research Institute hat sich einmal den Preisverfall für menschliche Genome angeschaut. Es sieht also ganz danach aus, als ob der Fortschritt im Bereich der DNA-Sequenzierung das Mooresche Gesetz noch ein gutes Stück hinter sich lässt.
Das sind nicht nur für Bioinformatiker, deren Stellen damit auf nächste Zeit gesichert sein dürften, gute Nachrichten. Sondern auch für alle die versuchen Krankheiten zu erforschen und etwas gegen Krankheiten zu unternehmen: So konnte das 5.2 Mb große Genom von dem momentan so gefürchteten EHEC-Stamm in einem darauf spezialisierten Labor in weniger als 3 Tagen durchgeführt werden. Auch auf dem Feld der menschlichen Genomik tut sich etwas, denn 10 Jahre nach Veröffentlichung des ersten Genoms ist auch klar: Mit einem Genom alleine (oder auch einer Hand voll) kann man wenig machen. Mehr Genome und auch mehr phänotypische Merkmale sind nötig, um mehr aus den Rohdaten erkennen zu können. Und genau daran wird bereits fleissig gearbeitet. Einer der Vorreiter auf diesem Feld der Genomik ist George Church, dessen Personal Genome Project sich zum Ziel gemacht hat, möglichst viele Individuen (aktuelles Ziel: 100.000 Teilnehmer) zu sequenzieren und die Daten, zusammen mit phänotypischen Eckdaten, zu veröffentlichen.
Bislang gibt es allerdings noch keine fertigen Genome, sondern nur Genotypisierungen (dazu später mehr). Auch wenn bislang noch vergleichsweise wenige, komplette Genome verfügbar sind: Die Zeichen für Genomsequenzierungen stehen gut, nicht nur dank den Bestrebungen von Church. Optimistischen Schätzungen zufolge wird der Preis für eine komplette Genom-Sequenzierung irgendwann 2011/2012 auf die magische 1000 US Dollar-Marke fallen. Und die BioTech-Firma Illumina bietet eine persönliche Genomsequenzierung bereits heute für gute 10.000 US $ an. Damit wird eine solche Sequenzierung nicht nur für mehr Forscher erschwinglich, sondern kommt auch in eine Preisklasse, die eine direkte medizinische Verwendung ermöglicht. Bereits 2010 wurde ein 11 Monate altes Mädchen komplett sequenziert, mit dem Ziel die Ursache für ihr bislang nicht erklärbares Krankheitsbild herauszufinden. Und mit sinkenden Kosten wird man so etwas bald auch häufiger sehen.
Kein Wunder also, dass deshalb das Zeitalter der personalisierten Medizin herbeigeträumt wird und gar nicht mehr so fern erscheint. Wer würde nicht wollen, dass man bei der Behandlung von Krankheiten über die Genetik herausfinden kann, welche Medikamente aufgrund besonderer Genvarianten besonders gut wirken oder gar ernste Nebenwirkungen hervorrufen? Oder herausfindet, welche Behandlung bei dem eigenen Krebs besonders gut wirkt?
Während diese Form der personalisierten Medizin noch nicht vollends in der Realität angekommen ist: Firmen wie 23andme und deCODEme bieten schon jetzt sogenannte „Direct-To-Customer“ (DTC) Analysen des eigenen Genoms an. Einfach das Test-Röhrchen bestellen, reinspucken, zurücksenden, und ein paar Wochen später bekommt man seine Ergebnisse per eMail und auf der Firmenwebseite aufbereitet präsentiert. Statt einer kompletten Sequenzierung setzt man hier aber auf einzelne Mutationen, sogenannte Single Nucleotide Polymorphisms, die analysiert werden. Bei 23andme bekommt man für umgerechnet circa 120 € ungefähr 1 Million solcher Marker ausgewertet. Viele davon sind bereits durch Studien mit bestimmten Eigenschaften wie erhöhten Krankheitsrisiken, erwarteter Reaktion auf Medikamente und anderes assoziiert. Personalisierte Medizin light, sozusagen.
Mit immer mehr verfügbaren Daten steigt allerdings auch der Aufwand, diese auszuwerten an. Dank frei verfügbarer Daten bleibt dies aber nicht mehr nur Wissenschaftlern vorbehalten. Nicht nur das Personal Genome Project veröffentlicht seine Daten komplett, auch Kunden von DTC-Services entschliessen sich dazu, ihre Rohdaten komplett zu veröffentlichen. Die SNPedia – ein offenes Projekt von Freiwilligen die Literatur zu Markern und Co zusammenfasst – listet zur Zeit gute 40 Individuen auf, deren Daten man für eigene Analysen verwenden kann. Und ich bin mir sicher, dass es im Laufe der Zeit noch mehr werden.
Das eröffnet nicht nur ein ganz neues Potential zum Crowd-Sourcing à la Wikipedia. Sondern dürfte in naher Zukunft auch noch so manchen kreativen Umgang mit diesen Daten und damit spannenden, neuen Einsichten mit sich bringen. Und auch die Anbieter von DTC-Tests nutzen ihre Datenbestände bereits um damit Forschung zu betreiten. So konnten nicht nur alte Krankheits-Assoziationen durch ihre Datensätze ebenfalls nachgewiesen werden. Sie konnten damit auch neue Verbindungen zur Parkinson-Erkrankungen herstellen. Die Genetik, gepaart mit den sinkenden Kosten, wird die Medizin in naher Zukunft revolutionieren. Und bestimmt auch den einen oder anderen Nobelpreis abstauben. Wir können gespannt sein, wie und von wem diese neuen Möglichkeiten ausgereizt werden.
Rios, J., Stein, E., Shendure, J., Hobbs, H., & Cohen, J. (2010). Identification by whole-genome resequencing of gene defect responsible for severe hypercholesterolemia Human Molecular Genetics, 19 (22), 4313-4318 DOI: 10.1093/hmg/ddq352
Wheeler, D., Srinivasan, M., Egholm, M., Shen, Y., Chen, L., McGuire, A., He, W., Chen, Y., Makhijani, V., Roth, G., Gomes, X., Tartaro, K., Niazi, F., Turcotte, C., Irzyk, G., Lupski, J., Chinault, C., Song, X., Liu, Y., Yuan, Y., Nazareth, L., Qin, X., Muzny, D., Margulies, M., Weinstock, G., Gibbs, R., & Rothberg, J. (2008). The complete genome of an individual by massively parallel DNA sequencing Nature, 452 (7189), 872-876 DOI: 10.1038/nature06884
Eriksson, N., Macpherson, J., Tung, J., Hon, L., Naughton, B., Saxonov, S., Avey, L., Wojcicki, A., Pe’er, I., & Mountain, J. (2010). Web-Based, Participant-Driven Studies Yield Novel Genetic Associations for Common Traits PLoS Genetics, 6 (6) DOI: 10.1371/journal.pgen.1000993
Do, C., Tung, J., Dorfman, E., Kiefer, A., Drabant, E., Francke, U., Mountain, J., Goldman, S., Tanner, C., Langston, J., Wojcicki, A., & Eriksson, N. (2011). Web-Based Genome-Wide Association Study Identifies Two Novel Loci and a Substantial Genetic Component for Parkinson’s Disease PLoS Genetics, 7 (6) DOI: 10.1371/journal.pgen.1002141