Portugal: Das Problem mit dem Geld
Im Zuge des aktuellen Bloggewitterrs zur Fußball-EM 2016 stelle ich heute eine Publikation aus Portugal vor.

Auf der einen Seite möchte ich dabei natürlich die Experimente und deren Ergebnisse vorstellen. Auf der anderen Seite möchte ich allerdings zunächst feststellen, dass ich mich ganz besonders über einen portugiesischen Artikel freue. Die allermeisten Artikel kommen heute natürlich mit großem Abstand aus den USA, nicht wirklich dicht gefolgt von China. Das liegt sicherlich auch an der schieren Größe und Fülle an wissenschaftlichen Instituten dieser Länder. Aber ein großer Faktor spielt dabei eben auch Geld, das in Portugal in den letzten Jahren im öffentlichen Sektor durch die Sparauflagen der EU nicht besonders üppig geflossen sein dürften. Und ohne Geld kann man in der Wissenschaft noch so interessante Ideen haben, wenn man keine eigenen Vorarbeiten vorweisen kann, wird es mit der Bewerbung um öffentliche Fördergelder nicht klappen. Wer kein Geld hat, wird vermutlich auch keins bekommen. Daher hat es mich sehr gefreut, als ich in der Danksagung des Artikels folgenden Satz gelesen habe: “We also thank Daniel Voytas and Adam Bogdanove for the kind gift of the TALEN Golden Gate kit, … .” Der hier erwähnte Daniel Voytas und sein Kollege Adam Bogdanove sind die führenden Wissenschaftler aus dem Bereich der artifiziellen TALE-Proteine, die ein Kit für den Zusammenbau von TALE-Proteinen über die Plattform Addgene vertreiben, dass kurz nach der Veröffentlichung bereits zu dem am meisten gekauften Vektoren auf der Platform zählte. Über die Non-Profit-Plattform Addgene können Wissenschaftler weltweit ihre selbst gebauten Vektoren mit anderen Wissenschaftlern teilen. Das Kit von Voytas und Bogdanove kostet “nur” 425 US$, was allerdings für eine kleine, nicht gut finanzierte Arbeitsgruppe ziemlich viel Geld bedeutet. Dass die beiden ihr Kit verschenkt haben, ist schon eine bemerkenswerte Unterstützung, sie sind dafür auch nicht als Koautoren auf dem Paper aufgeführt. Und das finde ich genauso bemerkenswert. Gut, die beiden brauchen die Zitate nicht mehr, aber ich kenne das selbst auch ganz anders: “Klar verrate ich euch meine Geräteeinstellungen, aber dafür kommen ich meine x weiteren Doktoranden dann auf dein Paper.”. Das ist leider weiter verbreitet, als man sich wünschen würde – Richtlinien zur guten wissenschaftlichen Praxis hin oder her.
Aber darum soll es ja gar nicht gehen, sondern um die Idee der bereits erwähnten portugiesischen Arbeitsgruppe. Und in der geht es um HIV. Genauer gesagt, geht es um einen Weg um die HI-Viren aus den Immunzellen in denen sie sich vertsecken, herauszulocken. Das hinterhältige an HIV ist ja bekanntermaßen, dass sie sich in die DNA von ruhenden Immunzellen einnisten und dort darauf warten sich immer wieder neu zu bilden. Besonders die langlebigen CD4+-T-Zellen (T-Gedächtniszellen) bilden das HIV-Reservoir, das dafür sorgt, dass bisher keine Heilung von HIV möglich ist. Zum Glück gibt es heute sehr potente antivirale Mittel, die die Viruslast im Blut unter das Detektionslevel drücken können – sofern man sie denn bekommen kann. Es gibt bereits viele verschiedene Ansätze um HIV zu aktivieren, u.a. Cytokine, Antikörper, Histon-deaetylasehemmer (HDAC) oder das Medikament Vorinostat.
Den Artikel den ich mitgebracht habe, verwendet eine neue Methode, und zwar meine heißgeliebten TALE-Proteine. Man kann nämlich nicht nur Nukleasen – also Proteine, die DNA schneiden – damit bauen, sondern auch andere DNA-beeinflussende Proteine. In diesem Fall benötigen wir ein Protein, das die genomischen Sequenzen des HI-Viruses aktiviert, also einen Transkriptionsfaktor, oder genauer einen Transkriptionsaktivator.
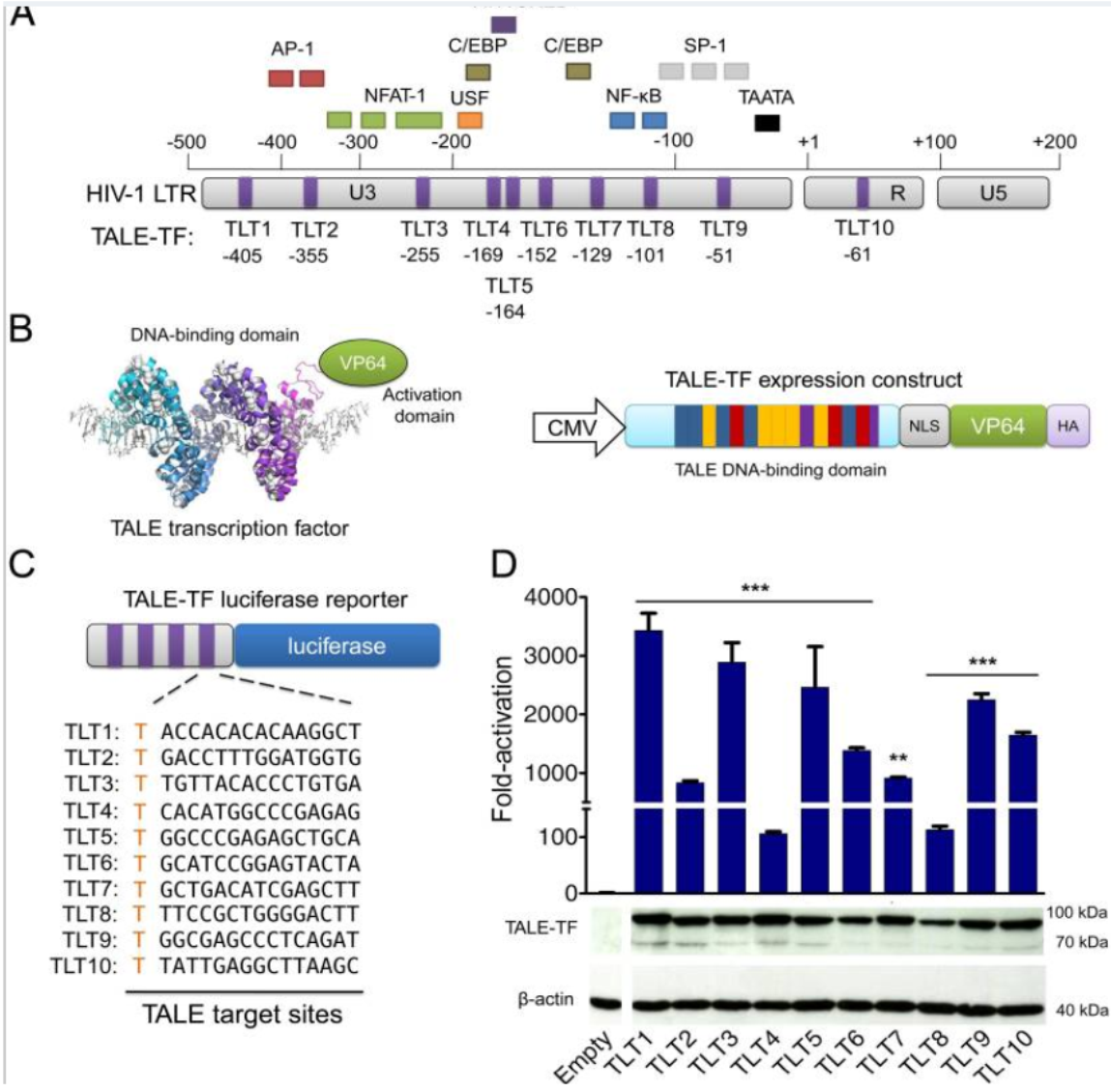
Und das haben sie wie folgt gemacht. Oben in der Abbildung in Teil A sehen wir den Long-Terminal-Repeat von HIV (HIV-1 LTR). LTRs sind Sequencen, die HIV, oder andere Viren, benötigen, um sich selbst in die DNA ihres Wirts einzubauen und sich anschließend wieder selbst auszuschleusen. LTRs flankieren die viralen DNA-Sequenzen links und rechts. Über der HIV-1 LTR sind die Bindungsstellen verschiedener körpereigener humaner Transkriptionsfaktoren gezeigt (C/EBP, AP-1 etc.). Und darunter, bezeichnet mit TLT-1 bis TLT-10 sind die selbst gebauten TALE-Transkritptionsfaktoren zu sehen. Teil B der Abbildung zeigt, wie so ein TALE-TF aufgebaut ist. Er besteht aus der DNA-Bindedomäne, dem TALE-Teil, der als Bändermodell in lila und blau dargestellt ist und an die graue DNA bindet. Der zweite Teil ist die Aktivierungsdomäne VP64, die einfachheitshalber nur symbolisch gezeigt ist. Rechts daneben ist die Struktur der TALE-TFs noch einmal in einer systematischen Abbildung gezeigt. Jedes der bunten Kästchen repräsentiert eine der vier DNA-Basen, ATGC, gefolgt von VP64. NLS bezeichnet das Kern-Lokaliserungssignal, ohne dass der der selbst gebaute Transkriptionsfaktor nicht in den Zellkern finden würde, wo er dann über den TALE-Teil an die virale LTR-Sequenz bindet und so über VP64 das Ablesen der HIV-DNA aktiviert. HA steht für Hemagglutinin und ist ein sogenannter Tag, also eine Markierung, die genutzt werden kann um das Protein später aufzureinigen oder sichtbar zu machen. CMV schleißlich bezeichnet den Promoter, der wiederum benötigt wird, damit der TALE-TF überhaupt in der Zelle abgelesen und anschließend das entsprechende Protein gebildet werden. Jetzt haben wir allerdings noch keine Information darüber, wie gut die 10 dargestellten TALE-TFs überhaupt DNA binden, bzw. HIV aktivieren werden. Das lässt sich bisher leider nur bedingt vorhersagen und muss daher vorher erprobt werden. Wie das prinzipiell gemacht wurde, zeigt Teil C der Abbildung. Hier wird die DNA-Sequenz an die der TALE-Teil bindet, genommen und mit der Luciferase-Sequenz verbunden. Das Ganze nennt sich dann Luciferase-Reporter-Konstrukt und ist eine sehr gängige Labor-Methode um regulatorische DNA-Sequenzen und ihre Aktivatoren zu untersuchen. Man spricht dann davon, dass die Luciferase unter der Kontrolle der jeweiligen DNA-Sequenz steht, d.h., bindet hier ein geeigneter Transkriptionsfaktor, wird die Luciferase aktiviert, abgelesen und erfüllt dann ihre biologische Funktion und fängt an zu leuchten. Dieses optische Siganl kann dann ausgelesen werden. Bringt man dieses Luciferase-Reporter-Konstrukt gemeinsam mit den einzelnen TALE-TF in Zellen ein, kann anhand der Intensität der gemessenen Bioluminsezenz bestimmt werden, wie gut die einzelnen TALE-TFs tatsächlich funktionieren. Das ist schließlich in Teil D der Abbildung gezeigt. Ganz links ist der leere Vektor aufgetragen (empty), hier wurde die Luciferase aber kein TALE-TF in die Zelle eingebracht und sie fängt auch nicht von selbst an sich abzulesen und zu leuchten. Daneben sieht man dann, dass die 10 TALE-TFs doch eine sehr unterschiedliche Aktivierungsgüte besitzen. Interessant dabei ist, dass die Nummern 4 und 8, zwar am schlechtesten abschnitten, aber mit Sequenzüberschneidungen mit den endogenen Transkriptionsfaktoren C/EBP and NF-κB besitzen. Diese nativen TFs könnten also durchaus zur Aktivierung von HIV beitragen. Unter der Grafik ist dann noch gezeigt, dass die TALE-TF Proteine tatsächlich gebildet wurden. Hier wurde der HA-Tag genutzt um die Proteine im Western Blot sichtbar zu machen, Aktivin dient dabei zur Positivkontrolle und wird standardmäßig immer mit angegeben.
Die selbst gebauten TALE-TFs funktionieren in der theoretischen Praxis also schonmal ganz gut. Wie sieht es aber mit ihrer Fähigkeit HIV zu aktivieren aus? Dazu wurde ein Zellkulturmodell verwendet, das für die Untersuchung von latenten HIV-Infektionen genutzt wird. Die Zellen tragen die HIV-Sequenz in ihrem Genom und sind so verändert, dass sie anfangen GFP zu bilden, also grün fluoreszieren, wenn HIV aktiviert wird.

Im oberen Teil der Abbilung (Figure 3A) sieht man, wie unterschiedlich stark die TALE-TFs in der Lage sind HIV zu aktivieren und dass die Ergebnisse aus dem Luciferase-Assay sich auch nicht unbedingt exakt so im Zellkulturmodell widerspiegeln. Als Positivkontrolle wird hier das Cytokin TNF und der virale HIV Transkriptionsaktivator Tat verwendet, die beide sehr viel potenter HIV aktivierten als die TALE-TFs. Wurden allerdings Komninationen der TALE-TFs verwendet (TLT6-7 etc.) konnten synergistische Effekte beobachtet werden und beinahe die Aktivierungsgüte von TNF erreicht werden. Um das Ganze abszuschließen wurden zusätzlich noch die TALE-TFs in Kombination mit einer der Eingangs erwähnten in der Praxis verwendeten Medikamente zur viralen Transkriptionsaktivierung getestet. Hier wurde HDAC verwendet und wie man im zweiten Teil der Abbildung (Figure 4) sehen kann, erhöht die Kombination mit den TALE-TFs die HIV-Aktivierung erheblich und zwar über das Niveau der TNF-vermittelten HIV-Aktivierung.
Ob es einmal eine therapeutische Anwendung hierfür geben wird, sei mal dahingestellt. Aber die Ergebnisse sind auf jeden Fall vielversprechend und ein interessanter neuer Ansatz. Und vielleicht bilden Sie ja sogar die Grundlage für den Erhalt eines fetten EU-Grants, der den Standort der portgiesischen Grundlagenforschung weiter stärken wird. Forca Portugal!
–
Lust auf mehr Wissenschaft aus Portugal? Der Nature Index, eine große Datenbank über Publikationen aus vielen Ländern und Instituten, gibt Ihnen einen Überblick über die dortige Forschungsszene.


Für HIV wird es bald eine Gentherapie geben – das ist beim gegenwärtigen Fortschritt (mehrere erfolgreiche Gentherapien der Hämophilie B und der Leberschen Amaurose) und der Tatsache, dass es mehrere Arbeitsgruppen gibt, die HIV mit gentherapeutischen Mitteln angehen, fast sicher.
Ob die Methode der HIV-Aktivierung die hier beschrieben wird, eine Rolle spielt, kann man im Moment nicht wissen (der Laie jedenfalls kann das nicht wissen, die Eingeweihten vielleicht schon).
Die Forscher die den oben zitierten Artikel geschrieben haben, arbeiten an der Universität Lissabon. Nur gerade von der Autorin, die als dritte auf der Autorenliste konnte ich ein (sogar mehrere) Lebenszeichen, entdecken, beispielsweise unter ResearchGate Mariana Santa-Marta
Da stimme ich absolut zu! Bereits vor 2 Jahren gab es erste klinische Versuche in den USA mit 12 HIV Patienten:
http://www.nature.com/news/gene-editing-method-tackles-hiv-in-first-clinical-test-1.14813
Zwar wurden hier “nur” Zinkfingernukleasen und nicht die neueren Methoden TALEN oder Crispr/Cas9 verwendet, aber so eine Studie ja auch nicht mal eben so aus dem Boden gestampft. HIV könnte vielleicht wirklich das erste Ziel groß angelegter klinischer Studien zum Genome Editing sein.
Achso und zu den Autoren: laut Autorenliste residieren nur 3 der 6 Autoren in Portugal, der Rest u.a. in Kalifornien. Und was die Lebenszeichen angeht, kann es durchaus sein, dass das Forscherteam, nunja, nicht mehr komplett ist: “Dedicated to the memory of Carlos F Barbas III.”