Neue Impftechnik könnte vor HIV Infektion schützen
BLOG: ImmunoLogisch

Amerikanischen Forschern ist es gelungen HIV Neuinfektionen über das Blut oder die Vaginalschleimhaut in Mäusen zu verhindern. Hierbei testeten die Wissenschaftler eine neue Impftechnologie namens „vektorisierte Immunprophylaxe“ oder kurz VIP. Diese Forschungsergebnisse sind von besonderer Relevanz für den Menschen, da zum einen Mäuse mit einem humanisierten Immunsystem eingesetzt wurden und zum anderen HI-Virusstämme verwendet wurden, mit denen sich Menschen infizieren können.
HIV löst die Immunschwächekrankheit AIDS aus, an deren Folgen bisher über 36 Millionen Menschen gestorben sind. Jeden Tag infizieren sich circa 6300 Menschen mit HIV (beinahe 263 Menschen pro Stunde). Nach effektiven Schutzmaßnahmen, wie Impfstoffen, wird fieberhaft geforscht. Die spezifischen Eigenschaften des HI-Virus machen es den Forschern jedoch schwer, ein wirkungsvolles Vakzin zu entwickeln.
Es gibt zwei Impfstrategien: die aktive und die passive Immunisierung. Bei ersterer wird das Immunsystem ‚aktiv‘ zur Bildung von Abwehrmechanismen angeregt, indem abgeschwächte oder Bruchstücke von Erreger gespritzt werden (z.B. Impfung gegen Masern). Bei der passiven Immunisierung bleibt das eigene Immunsystem ‚passiv‘, denn es werden Erreger-neutralisierende Antikörper gespritzt, die entweder gentechnologisch hergestellt wurden oder von einem anderen Körper/Organismus stammen.
Die aktive Immunisierung scheitert bei HIV, da ein abgeschwächter Impfstoff zu große Risiken einer Infektion birgt und ein Impfstoff, der Virus-Bruchstücke enthält, keine schützende Immunantwort aufbaut. Die passive Immunisierung, zu der die vektorisierte Immunprophylaxe gehört, ist jedoch vielversprechend.
Bei der vektorisierten Immunprophylaxe bekämpft so zu sagen ein Virus den anderen, genauer: der Adeno-assozierte-Virus (AVV) den HI-Virus!
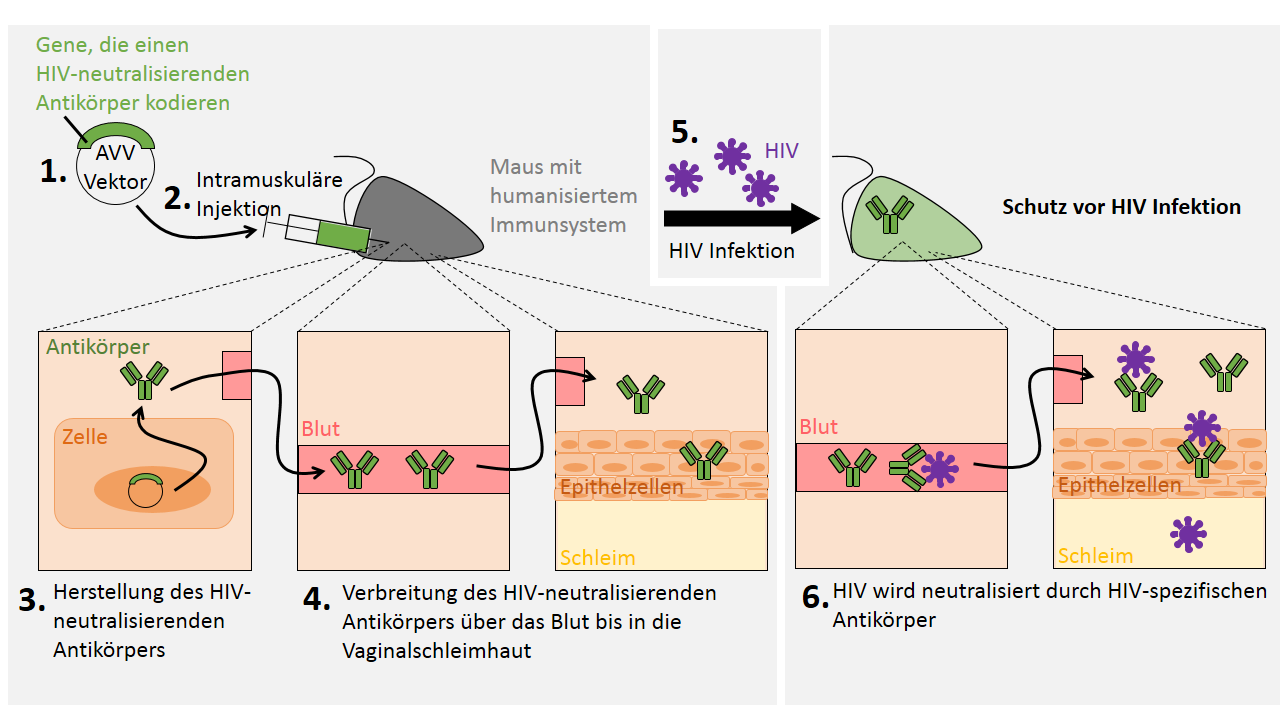
Wie soll das gehen? AAV ist ein kleiner Virus der zwar Menschen infiziert aber keine Krankheiten auslöst. Wie auch krankmachende Viren schleust er sein Genom in Wirtszellen ein und veranlasst diese dazu die Genprodukte, die auf der Virus-DNA kodiert sind, herzustellen. Da die AAV-DNA keine Gene enthält, die dem Menschen gefährlich werden können, benutzen die Forscher diese als Vektor (lat. vector „Träger, Fahrer“). In dieser Studie schleusten die Wissenschaftler als erstes Gene in die AAV-DNA ein, die einen neutralisierenden HIV-Antikörper kodieren (1). Den so veränderten AAV Vektor spritzten sie dann in Muskelgewebe einer Maus mit humanisiertem Immunsystem (2). Daraufhin infizierte der AA-Virus Mauszellen und veranlasste diese zur Herstellung eben jener neutralisierenden HIV-Antikörpern (3). Diese verteilen sich dann über das Blut und erreichen somit auch die Vaginalschleimhaut (4). Die Forscher versuchten nun diese Mäuse über das Blut oder den Genitaltrakt mit HIV zu infizieren (5). Die über das AAV erzeugten HIV-Antikörper verhinderten jedoch eine Infektion (6).
Diese Forschungsergebnisse machen Hoffnung auf eine neue Art der AIDS Prävention, allerdings darf man die anatomischen Unterschiede von Maus und Mensch nicht außer Acht lassen. Auch widerspiegelt eine Maus mit einem humanisierten Immunsystem nicht komplett das menschliche. Es bleibt abzuwarten, ob mit einer vektorisierten Immunprophylaxe beim Menschen ähnliche Ergebnisse erzielt werden können wie bei Mäusen. Ein kritischer Faktor wird zum Beispiel sein, eine HIV-neutralisierende Antikörperkonzentration im Menschen aufzubauen, die effektiv vor einer HIV Infektion schützen kann.
Quellen
Vektored immunoprophylaxis protects humanized mice from mucosal HIV transmission by Balazs et al. published in Nat Med 2014 (Vol 20, Nr 3)
http://www.amfar.org/about-hiv-and-aids/facts-and-stats/statistics–worldwide/


Die vektorisierte Immunprophylaxe kann als zu Gentherapien verwandten Methode aufgefasst werden. Das Therapie-Gen wird allerdings nicht in das menschliche Genom integriert sondern ist lediglich Bestandteil eines Virus, welches menschliche Zellen infiziert, sie zur Replikation der viralen Gene und der Produktion viraler Proteine veranlässt. Das Therapiegen welches Bestandteil des Virusgenoms ist, codiert für einen Antikörper gegen HIV, der dann von den menschlichen Proteinfabriken produziert wird.
Möglicherweise ist es nicht vollkommen richtig diese Art der Impfung als passiv zu bezeichnen. Beim passiven Impfen spritzt man Antikörper gegen den Krankheitserreger und diese Antikörper verlieren innert kurzer Zeit ihre Wirkung, weil sie ausgeschwemmt und abgebaut werden. Bei der vektorisierten Immunprophlaxe jedoch werden neue therapeutische Antikörper erzeugt solange der Virus sich im Körper vermehrt. Die vektorisierte Immuntherapie könnte also wesentlich länger wirksam sein als es eine klassische passive Impfung ist.
Überhaupt zeichnen sich nun auf vielen verschiedenen Gebieten wirksame Gentherpien ab. So wurde kürzlich berichtet, dass extrakoroporal durch Genmodifikation immun gegen HIV gemachte T-Lymphozyten unter günstigen Umständen den HIV-Virus vollkommen eliminieren können.
T-Lymphozyten können auch so genmodifiziert werden, dass die Krebszellen angreifen, eine Methode, die kürzlich an Patienten mit seltenen Formen von Blutkrebs im Terminalstadium ausprobiert wurde und zu Remissionen bis 80% führte.
Welche Mauszellen produzierten den neutralisierenden HIV-Antikörper? Was passiert wenn man statt Muskelgewebe das Knochenmark infiziert um B-Zellen mit zusätzlichen Waffen aufzurüsten?
@ Joe Dramiga
Die Wissenschaftler haben den AAV-Vektor in den Wadenmuskel der Mäuse gespritzt. Bereits in früheren Publikationen wurde berichtet, dass der AAV-Vektor zuverlässig Muskelzellen infizieren kann. Vermutlich wurde daher diese Stelle zur Injektion gewählt.
In der Tat wäre die Idee B-Zellen zu infizieren naheliegend, da B-Zellen die einzige Zellen sind die auf natürlichem Weg Antikörper herstellen können. Die B-Zellen entwickeln sich im Knochenmark von hämatopoetischen Stammzellen.
Hämatopoetische Stammzellen sind ein interessantes Ziel um künstlich Gene einzuschleusen (Gentherapien) auf Grund ihrer Fähigkeit sich in zahlreiche Blutzelltypen zu entwickeln. Allerdings ist die gezielte Infektion von hämatopoetische Stammzellen für Gentherapien nach wie vor eine Herausforderung, da sieh häufig zu niedrigen Infektionsrate führt. Ähnlich verhält es sich mit den B-Zellen: Genprodukte, kodiert auf viralen Vektoren, lassen sich schwer in B-Zellen einschleusen. Benutzt man allerdings einen Virus der sich natürliche zu B-Zellen „hingezogen fühlt“ kann man B-Zellen erfolgreich transduzieren. Ein solcher Virus ist der Epstein-Barr Virus (EBV), der zu der Familie der Herpesviren gehört. Allerdings ist der EBV an der Entstehung zahlreichen menschlichen Erkrankungen beteiligt. Einen Einsatz von diesem Virus in der Gentherapie machen aufwendige genetische Veränderungen und Sicherheitskontrollen notwendig.
Kann man die B-Zellen nicht ex vivo infizieren, mit Positiv-Selektion anreichern und dann wieder in den Körper injizieren?
Solche ex vivo Gentransfers (wo Zellen außerhalb des Körper „manipuliert“ werde) wurden bereits erfolgreich durchgeführt. Hierbei muss man allerdings darauf achten autologe (von ein- und derselben Person stammende) Zellen zu verwenden. Hellenbrand et al. (Gene Therapy 2006) z.B. zeigen in einer Studie, dass EBV-basierte Vektoren erfolgreich Gene in menschliche B-Zellen einschleusen können. Sie spekulieren, dass diese Methode Potential für die Entwicklung zukünftiger Antitumor-Impfungen hat.